- Йога начинающим видео
- Хулахуп танец видео
- Смотреть моя тренировка видео
- Видео тренировки александра емельяненко
- Как правильно крутить обруч на бедрах видео
- Тренировки в кудо видео
- Тренировки рой джонса видео
- Йога онлайн смотреть видео
- Тренировки костя дзю видео
- Видео тренировки роя джонса
- Видео спинальной
- Айенгар йога видео
- Йога для женщин на видео
- Правильно крутить обруч видео
- Плиометрические отжимания видео
- Новости

Управление Здравоохранения Евпаторийского городского совета (С)2011
67 гостей
A Protocol for Analyzing Hepatitis C Virus Replication
Вірус гепатиту С є РНК-вірус. Таким чином, для генетичної маніпуляції мети HCV геномної кДНК була клонована в плазмідний вектор бактеріальної. Т7 РНК-полімераза послідовність промотора була введена безпосередньо перед 5'-кінці генома ВГС. Загальна схема аналізу HCV процесу представлена на малюнку 1. Для генерації HCV геномної РНК з точним 3 'кінці, геном ВГС містить плазміди розрізають Xba I рестріктази і згенерований одноцепочечной звис був притупляються з маш нуклеазами. Якість линеаризованной плазміди HCV оцінювали електрофорезом в агарозному гелі (фіг. 2В). HCV ДНК піддавали РНК-полімерази Т7 опосередкованої транскрипції в пробірці, і отриманий РНК отримували один продукт в 9,6 т.п.о. (рис. 2в).
Ми протестували кінетики росту в intragenotype 2а HCV (рис. 60, 3). В Хух-7.5.1 клітини електропорації з в пробірці транскрибується РНК дикого типу (WT) і полімерази нульових вірусів. Ми оцінили вірусну сенс реплікації генома за допомогою ОТ-КПЦР. Результати показали, що вірус WT реплікації генома ефективно (Фіг.3 і 3В). Дикого типу виставлені 2:59 журналу високий рівень реплікації генома в порівнянні з Поль-вірусу. Вірус WT виробляє білок NS3 (фіг.3С), який бере участь у розщепленні білка вірусної протеази (активність) і реплікації генома (геліказа активності). Також вірус WT висловив NS5A білок за оцінкою імунофлуоресцентній (рис. 3D). NS5A білок є частиною ВГС РНК реплікази комплексу. Для візуалізації реплікації вірусного генома, ми досліджували наявність двухцепочечной (DS) РНК ВГС з використанням антитіла, які специфічно розпізнає дсРНК. У HCV посилення генома, смислова ланцюг РНК сopied в антисмислової геном, таким чином двухцепочечной РНК проміжні присутні в цитоплазмі інфікованої клітини. Білок NS5A і дсРНК ко-локалізується в клітинній цитоплазмі (рис. 3D) з WT трансфекції клітин пропонуючи активну реплікацію вірусу. Взяті разом, вірус WT створений активної реплікації вірусу в трансфікованих Хух-7.5.1 клітин.
Прогрес в дослідженнях ВГС був обмежений через відсутність інфекційного системі культури клітин. Відкриття JFH-1 штаму ВГС і подальшої характеризації химерних лабораторних штамів дозволяє досліджувати весь цикл реплікації HCV в клітинній культурі в тому числі вірусного входу, переклад РНК, РНК реплікації і формування інфекційного вірусного потомства. Для оцінки титру ВГС і De Novo інфекційність, ми щепили стільникового-культуральних супернатантів знайденим HCV РНК трансфекованих клітин. ВГС візуалізували шляхом виявлення NS5A білок HCV і рассчітиваетсятітр вірусу шляхом підрахунку інфекційних вогнищ (рис. 4). Ми розглянули ізольовані кластер з мобільних телефонів (більше 2 клітини) позитивний результат на NS5A як єдиний фокус. Результати показали, що вірус є інфекційним WT і виробляє понад 10 4 осередки утворюють одиниць / мл інфекційного частки.
Ми також встановили репортер вірус гепатиту приховування Renilla люціферази (Rluc) ген-репортер (Малюнок 5A). Репортер HCV може бути використаний для тестування велика кількість мутантних вірусів, а також для високого вмісту скринінгу. Тут ми представляємо оцінку зростання фенотипів WT і Поль-репортер вірусів. Якщо вірусний геном реплікується, активність люціферази збільшить понаднормові після трансфекції. Підвищені рівні реплікації генома можуть бути виведені з підвищеної активності люціферази. Таким чином, активність люціферази побічно забезпечує вимір рівня реплікації генома. Лізати зібрані з WT або Pol-VIRAL РНК трансфіковані клітини в зазначені моменти часу відчували на люціферазних діяльності. О 6 год після трансфекції, як WT і Pol-віруси були подібні заходи люціферази, вказуючи подібний рівень вхідного трансфіковані РНК, які були переведені (рис. 5Б). Однак через 48 годин і 96 годин після трансфекції, вірус WT виставлені збільшені рівні реплікації генома в порівнянні з Поль-вірусу. Крім того, вірус WT проводиться вірусний білок NS3, як перевірено за допомогою Вестерн-блот (фіг. 5C). Згодом, ми протестували інфекційність WT і Поль-репортер вірусів шляхом посіву наївні Хух-7.5.1 клітини з безклітинних супернатантах, зібраних з 48 годин і 96 годин після трансфекції клітинних культурах. Pol-вірус мав активність люціферази базового рівня, в той час як вірус WT було 2-3 журналу високий рівень реплікації, що і Поль-репортера вірусу (рис. 5D). Результати показують, що у нас є надійний ВГС інфекційне Cultu клітин Re системи.
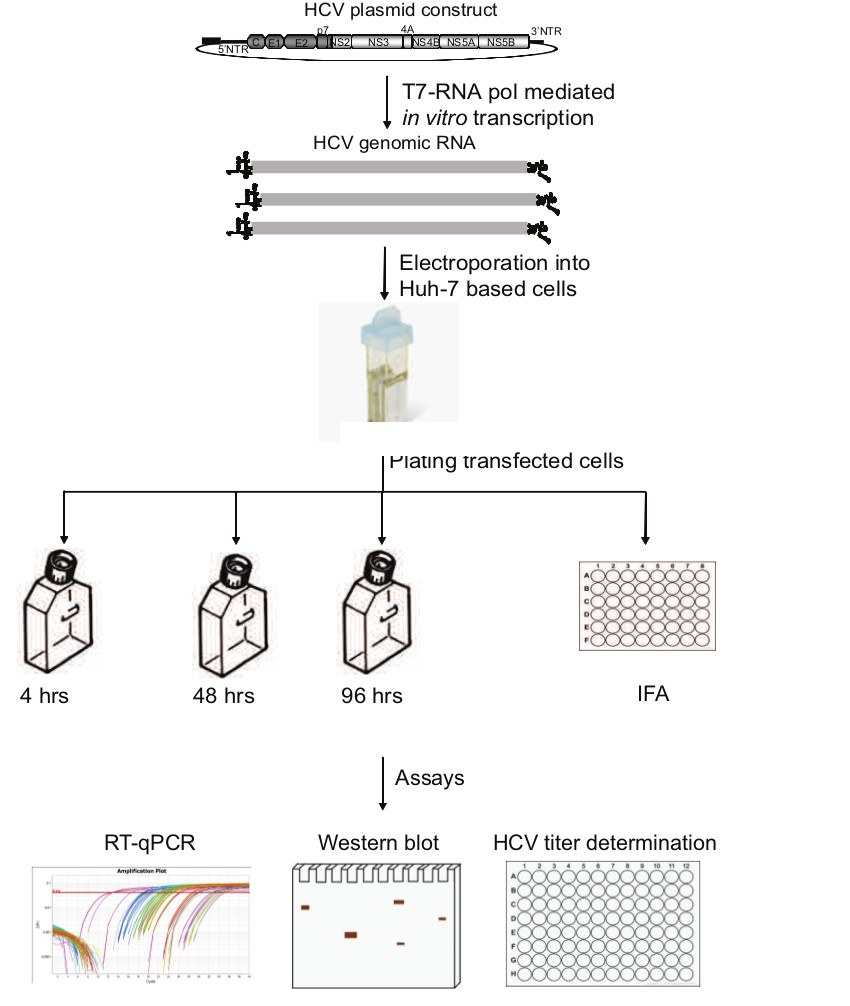
Малюнок 1. Загальна схема процесу аналізу реплікації ВГС. Лінеаризоване HCV плазміди конструкцію, яка містить РНК-полімерази Т7 промотор (T7P) піддається в пробірці транскрипції. Очищений РНК HCV геном електропорації в Huh-7.5.1 клітин і висівали в колби і 48-ямковий планшет. На 4 ч, 48 ч і 96 ч після трансфекції, клітинну РНК і культуральні супернатанти збирають з колб. Клітини з 48-ямкового планшета використовуються для збирання білка лизата і фіксуються для імунофлуоресцентного аналізу. Число Геном копія аналіз RT-КПЦР, вестерн-блот і вимірювання титр вірусу проводяться, щоб оцінити реплікацію HCV.
1362fig2highres.jpg "ширина =" 400 "/>
Малюнок 2. Виробництво HCV геномних РНК по транскрипції в пробірці, побудованих плазмідних ДНК. А) Геномна організація J6CF / JFH-1 intragenotype 2а химерних вірусів, FNX-ВГС і FNX-HCV-Поль нуль. Штам область J6CF (5'NTR в частині NS2) зображений темно-сірого кольору і деформації області JFH-1 (частина NS2 до 3'NTR) відображається в світло-сірий. NS5B полімерази мутація каталітичний домен (ДДГ, щоб AAG) позначається зірочкою. B) операцій, пов'язаних генерації лінеаризовану плазміди HCV. Гель картина показує лінеаризовані, з тупими кінцями плазміди ДНК, вироблені Xba I і маш нуклеазами, готові до в пробірці транскрипції. 0,8% агарозному гелі був використаний для вирішення ДНК. С) Гель картина зображує HCV генома РНК, вироблені в пробірці транскрипції з використанням Т7 РНК-полімерази системи. WT: дикого типу; Pol-полімеразна нуль; М: маркер.
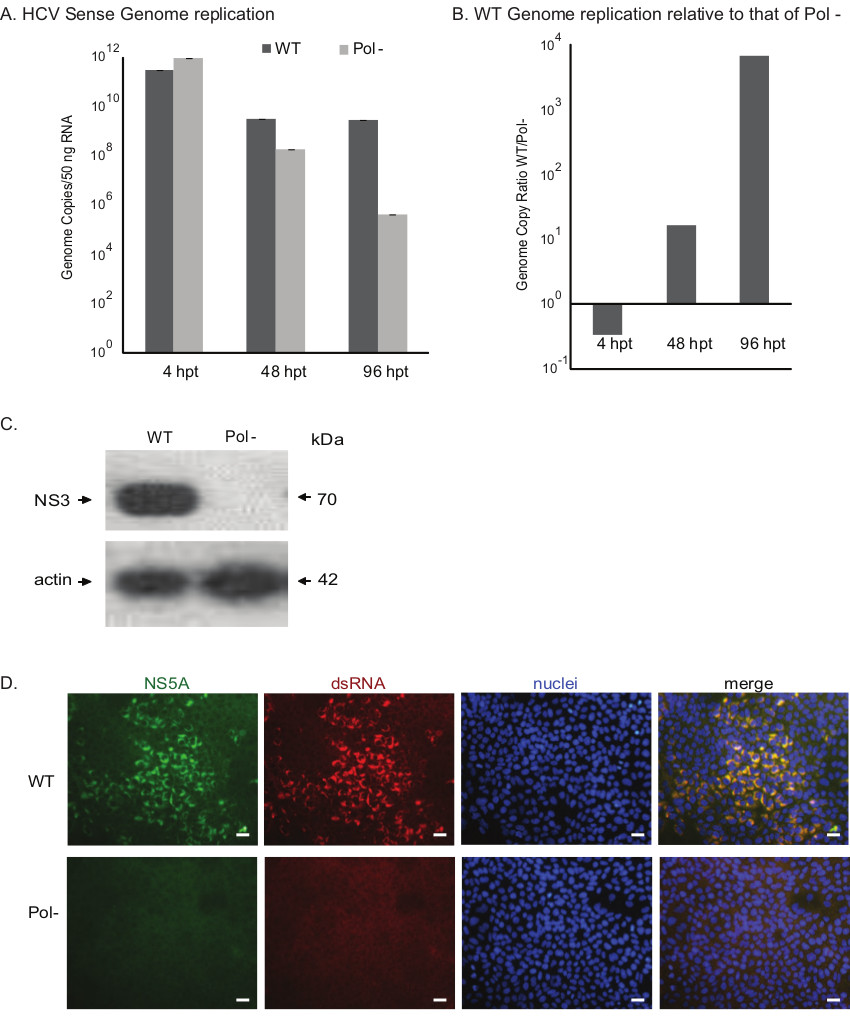
Малюнок 3. Оцінюючи фенотип зростання конструкцій HCV. А) Оцінка кінетики реплікації генома дикого типу (WT) і полімеразної нуль (Pol-) вірусів. Цифри геном копіювання з смисловий РНК нитки оціненої за допомогою ОТ-кількісної ПЛР представлені в гістограмі. Вірусний геном копії Pol-вірусу знизилася за період часу з зазначенням реплікації з дефіцитом фенотип. B) Відносний рівень реплікації генома дикого типу ВГС у порівнянні з Поль-вірусу. C) Вестерн-блот аналіз експресії білка ВГС. Білок NS3 HCV виявляється і бета-актину використовується в якості клітинного контролю. D) імунофлуоресцентного аналізу для дослідження реплікацію вірусу. На 96 годин після електропорації клітини фіксували і піддавали IMMunostaining для NS5A ВГС білка і двухцепочечной РНК (DS РНК), маркера для проміжних реплікації РНК ВГС. Ядра були візуалізовані з Hoechst пляма (Шкала бар 50 мкм). HPT :. годин після трансфекції Будь ласка, натисніть тут, щоб подивитися збільшену версію цієї фігури.
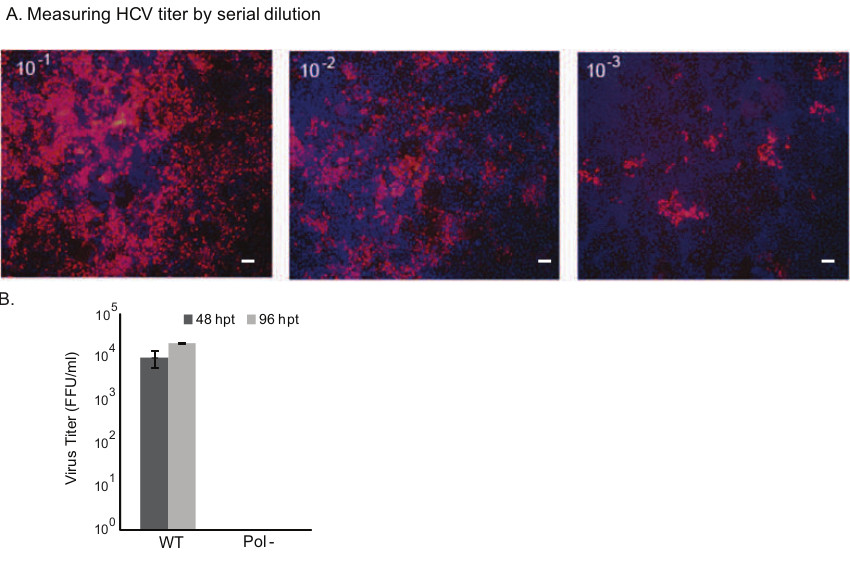
Малюнок 4. Розглядаючи інфекційність дикого типу HCV і вимірювання титру вірусу. А) Наївне Хух-7.5.1 клітини були використані для зараження досліджень. Безклітковий супернатант збирали в 48 і 96 годин після трансфекції (ТВД) РНК ВГС були піддані 10-кратного серійного розведення і додавали до клітин в 96-ямковий планшет тричі. 72 години після зараження, клітини фіксували і імунологічно фарбували для NS5A HCV білок. Клітини з NS5A позитивне забарвлення (червоний) заражені вірусом. Для оцінки вогнищ формуючого пристрою (ФФУ), позитивний осередки на найвищому розведенні були підраховані. Типові панелі наведені зображень (Шкала бар 100 мкм). B) Середні значення та стандартні відхилення титру вірусу в ФФУ на мілілітр показані на графіку. Полімеразної нуль мутант не виробляють інфекційних частинок. WT: дикого типу; Pol- :. полімеразної нуль Будь ласка, натисніть тут, щоб подивитися збільшену версію цієї фігури.
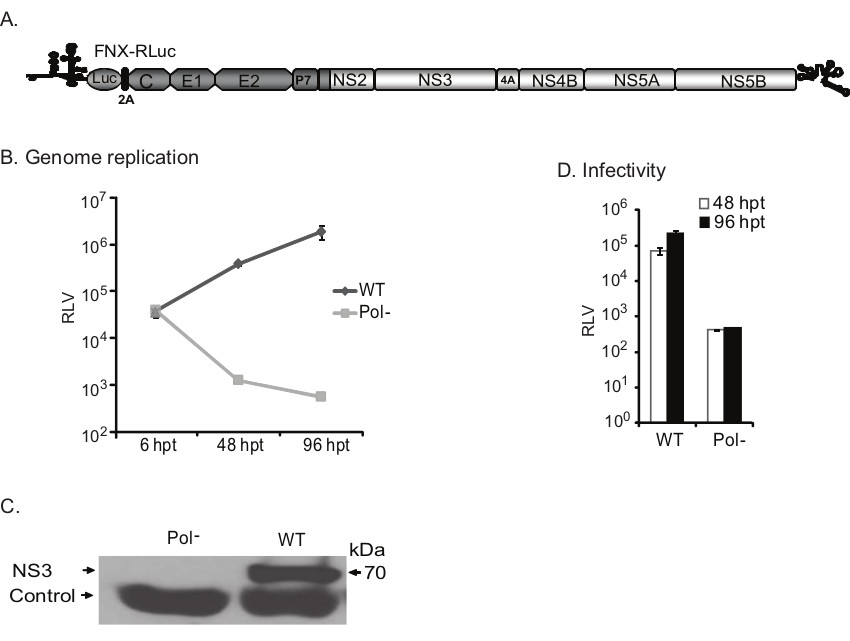
Малюнок 5. Оцінюючи реплікації генома і інфекційність репортера ВГС. А) мультфільм intragenotype 2а химерний вірус репортера представлений. Ген люціферази Renilla вставляється inframе між 5'NTR і серцевини. б) кінетика реплікації генома дикого типу і мутантних Pol-репортер вірусів за вказаною тимчасових точках після трансфекції показано на графіку. Білкові лізати збирали через 6 ч, 48 ч і 96 ч точок часу для вимірювання Renilla ферментативну активність люціферази. Середнє значення і стандартне відхилення обчислюється з трьох паралельних значень люціферазних Renilla (RLV) для кожного вірусу представлені на графіку. C) Вестерн-блот панель показує експресію білка ВГС NS3. Ні-специфічний антиген виявлений NS3 первинного антитіла діє як управління завантаженням. Дикого типу (WT) вірус репортер виробляє високий рівень білка NS3. D) аналіз інфекційності вірусу. Наївні Ха-7.5.1 клітини інокулював вбезклітинних надосадової рідини, отриманої з культури трансфікованих на 48 год і 96 год часу. Renilla люціферази діяльність інфікованих клітин були виміряні при 48 ч після інфекціі.Средніе значення зі стандартним відхиленням показані на графіку. Вірус Pol-репортер заражені клітини був тільки фоновий рівень активності люціферази, в той час як вірус WT репортер виставлені високий рівень інфекційної.


