- Йога начинающим видео
- Хулахуп танец видео
- Смотреть моя тренировка видео
- Видео тренировки александра емельяненко
- Как правильно крутить обруч на бедрах видео
- Тренировки в кудо видео
- Тренировки рой джонса видео
- Йога онлайн смотреть видео
- Тренировки костя дзю видео
- Видео тренировки роя джонса
- Видео спинальной
- Айенгар йога видео
- Йога для женщин на видео
- Правильно крутить обруч видео
- Плиометрические отжимания видео
- Новости

Управление Здравоохранения Евпаторийского городского совета (С)2011
67 гостей
Порушення білкового обміну
- § 185. Порушення азотистого рівноваги
- § 186. Порушення надходження, перетравлення і всмоктування білків в шлунково-кишковому тракті
- § 187. Порушення синтезу і розпаду білка
- § 188. Порушення обміну амінокислот
- § 189. Порушення кінцевих етапів білкового обміну
Частина друга. Типові патологічні ПРОЦЕСИ
Розділ XI. Патологічна ФИЗИОЛОГИЯ типове ПОРУШЕНЬ ОБМІНУ РЕЧОВИН
Глава 4. Порушення білкового обміну
Загальне уявлення про порушення білкового обміну можна отримати при вивченні азотистого рівноваги організму і навколишнього середовища.
§ 185. Порушення азотистого рівноваги
Порушення азотистого рівноваги проявляється у вигляді позитивного або негативного азотистого балансу.
Позитивний баланс азоту - стан, коли з організму виводиться менше азоту, ніж надходить з їжею. Спостерігається воно під час росту організму, при вагітності, а також після голодування, при надмірній секреції анаболічних гормонів (соматотропний гормон, андрогени та ін.) І при призначенні їх з лікувальною метою.
Анаболізму гормонів полягає в посиленні процесів синтезу білка в порівнянні з його розпадом. Такою дією володіють такі гормони.
- Соматотропний гормон підсилює окислення жиру і мобілізацію нейтрального жиру.
- Статеві гормони посилюють процеси синтезу білка.
- Інсулін полегшує перехід амінокислот через клітинні мембрани всередину клітин і, таким чином, сприяє синтезу білка і послаблює глюконеогенез. Нестача інсуліну веде до зниження синтезу білка і до збільшення глюконеогенезу.
Негативний азотистий баланс - стан, коли з організму виводиться більше азоту, ніж надходить з їжею. Негативний азотистий баланс розвивається при голодуванні, протеїнурії, інфекційних захворюваннях, травмах, термічних опіках, хірургічних операціях, при надмірній секреції або призначення катаболічних гормонів (кортизол, тироксин та ін.).
Катаболічна дію гормонів полягає в посиленні процесів розпаду білків у порівнянні з процесами синтезу. Такою дією володіють такі гормони.
- Тироксин збільшує кількість активних сульфгідрильних груп в структурі деяких ферментів - активуються тканинні катепсини посилюється їх протеолітичну дію. Тироксин підвищує активність амінооксідаз - збільшується дезаминирование деяких амінокислот. При гіпертиреозі у хворих розвивається негативний азотистий баланс і креатинурія.
- При дефіциті гормонів щитовидної залози, наприклад, при гіпотиреозі, недостатність катаболічного дії гормону проявляється у вигляді позитивного азотистого балансу і накопичення креатину.
- Глюкокортикоїдних гормони (кортизол та ін.) Підсилюють розпад білків. Витрата білків збільшується на потреби глюконеогенезу; при цьому також сповільнюється синтез білка.
Порушення обміну білків може бути результатом порушень:
- надходження, перетравлення і всмоктування білків в шлунково-кишковому тракті;
- синтезу і розпаду білків в клітинах і тканинах організму;
- проміжного обміну амінокислот;
- кінцевих етапів білкового обміну.
§ 186. Порушення надходження, перетравлення і всмоктування білків в шлунково-кишковому тракті
Розлади секреції окремих протеолітичних ферментів шлункового тракту, як правило, не викликають серйозних порушень білкового обміну. Так, повне припинення секреції пепсину з шлунковим соком не відбивається на ступеня розщеплення білків в кишечнику, але істотно впливає на швидкість його розщеплення і появи окремих вільних амінокислот.
Відщеплення окремих амінокислот в шлунково-кишковому тракті відбувається нерівномірно. Так, тирозин і триптофан в нормі отщепляются від білків вже в шлунку, а інші амінокислоти - лише під дією протеолітичних ферментів кишкового соку. Склад амінокислот у вмісті кишечника на початку і кінці кишкового перетравлення різний.
Амінокислоти можуть надходити в систему ворітної вени в різному співвідношенні. Відносний дефіцит навіть однієї незамінної амінокислоти утруднює весь процес біосинтезу білків і створює відносний надлишок інших амінокислот з накопиченням в організмі проміжних продуктів обміну цих амінокислот.
Подібні порушення обміну, пов'язані з запізненням відщеплення тирозину і триптофану, виникають при ахілії і субтотальної резекції шлунка.
Порушення всмоктування амінокислот може виникнути при патологічних змінах стінки тонкого кишечника, наприклад при запаленні, про теке.
§ 187. Порушення синтезу і розпаду білка
Синтез білка може бути порушений під дією різних зовнішніх і внутрішніх хвороботворних чинників:
- при неповноцінності амінокислотного складу білків, що надходять з їжею;
- при патологічних мутаціях генів, пов'язаних як з появою патогенних структурних генів, так і з відсутністю нормальних регулюючих і структурних генів;
- при блокуванні гуморальними факторами ферментів, що відають процесами репресії і депресії синтезу білка в клітинах;
- при порушенні співвідношення анаболічних і катаболічних факторів, що регулюють синтез білка.
Відсутність в клітинах навіть однієї незамінної амінокислоти припиняє синтез білка.
Біосинтез білка може порушуватися не тільки при відсутності окремих незамінних амінокислот, але і при порушенні співвідношення між кількістю незамінних амінокислот, що надходять в організм. Потреба в окремих незамінних амінокислотах пов'язана з їх участю в синтезі гормонів, медіаторів, біологічно активних речовин.
Недостатнє надходження в організм незамінних амінокислот викликає не тільки загальні порушення синтезу білка, але і вибірково порушує синтез окремих білків. Недолік незамінної амінокислоти може супроводжуватися характерними для неї порушеннями.
- Триптофан. При тривалому виключенні з харчового раціону у щурів розвивається васкуляризація рогівки і катаракта. У дітей обмеження триптофану в їжі супроводжується зниженням концентрації плазмових білків.
- Лізин. Відсутність в їжі супроводжується у людей появою нудоти, запаморочення, головного болю і підвищеної чутливості до шуму.
- Аргінін. Відсутність в їжі може привести до пригнічення сперматогенезу.
- Лейцин. Відносний надлишок його в порівнянні з іншими незамінними амінокислотами у щурів пригнічує ріст через відповідного порушення засвоєння изолейцина.
- Гистидин. Недолік його супроводжується зниженням концентрації гемоглобіну.
- Метіонін. Виняток його з їжі супроводжується жировим переродженням печінки, обумовленим недоліком лабільних метальних груп для синтезу лецитину.
- Валін. Недолік його веде до затримки росту, втрати маси, розвитку кератоз.
Замінні амінокислоти суттєво впливають на потребу в незамінних амінокислотах. Наприклад, потреба в метіоніні визначається вмістом цистину в дієті. Чим більше в їжі цистину, тим менше витрачається метіоніну для біологічного синтезу цистину.
Якщо в організмі швидкість синтезу замінної амінокислоти стає недостатньою, з'являється підвищена потреба в ній.
Деякі замінні амінокислоти стають незамінними, якщо вони не надходять з їжею, так як організм не справляється з швидким їх синтезом. Так, недолік цистину веде до гальмування росту клітин навіть при наявності всіх інших амінокислот в середовищі.
Порушення синтезу білка виникають при патологічної мутації структурних генів. Якщо в оперон синтезу навіть один зі структурних генів буде патологічним, то синтезована і-РНК несе помилкову інформацію про вид і місце включення однієї з амінокислот в молекулу білка. Таке порушення синтезу білка - гемоглобіну лежить в основі серповидноклітинної анемії (див. § 231).
Порушення синтезу білка можуть виражатися в генетично обумовленому припинення синтезу окремих видів білка: глобулінів (агаммаглобулинемия), ферментів. При відсутності ферментів синтезу кортикостероїдів (11-гідроксилази, 21-гідроксилази) розвиваються деякі види адреногенитального синдрому (див. § 328).
Припинення синтезу ферментів, що регулюють перетворення білків і амінокислот, веде до патологічних змін проміжного обміну білків і до порушень амінокислотного обміну.
§ 188. Порушення обміну амінокислот
Порушення дезамінування. Окислювальне дезамінування здійснюється в результаті послідовних перетворень амінокислот в реакціях переамінування і дезамінування:
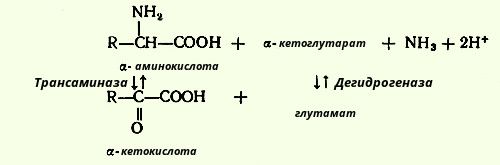
Амінокислоти за участю специфічних трансаміназ спочатку переамініруются з α-кетоглютарової кислотою. Утворюється кетокислоту і глютамат. Глютамат під впливом дегідрогенази піддається окислювальному дезамінування із звільненням аміаку і освітою α-кетоглютарат. Реакції оборотні. Таким чином утворюються нові амінокислоти. Включення α-кетоглютарової кислоти в цикл Кребса забезпечує включення амінокислот в енергетичний обмін. Окислювальне дезамінування визначає і утворення кінцевих продуктів білкового обміну.
З переамінуванням пов'язано освіту аминосахаров, порфіринів, креатину і дезамінування амінокислот. Порушення переамінування виникає при нестачі вітаміну В6, так як його форма - фосфопиридоксаль - є активною групою трансаміназ.
Співвідношення субстратів переамінування визначає напрямок реакції. При порушенні мочевінообразованія відбувається прискорення переаминирования.
Ослаблення дезамінування виникає при зниженні активності ферментів - аміноксідаз і при порушенні окислювальних процесів (гіпоксія, гіповітаміноз С, РР, В2). При порушенні дезаминирования амінокислот збільшується виділення амінокислот з сечею (аминоацидурия), зменшується мочевінообразованія.
Порушення декарбоксилирования. Декарбоксилирование амінокислот супроводжується виділенням СО2 й утворенням біогенних амінів.
У тваринному організмі декарбоксилюванню піддаються лише деякі амінокислоти з утворенням біогенних амінів: гістидин (гістамін), тирозин (тирамін), 5-гідрокситриптофан (серотонін), глютамінова кислота (гамма-аміномасляна кислота) і продукти подальших перетворень тирозину і цистину: 3,4 диоксифенилаланин (ДОФА, оксітірамін) і цістеіновая кислота (таурин) (рис. 31).
Біогенні аміни виявляють свою дію вже при малих концентраціях. Накопичення амінів у великих концентраціях є серйозною небезпекою для організму. У нормальних умовах аміни швидко усуваються під дією аміноксідази, яка окисляє їх в альдегіди:
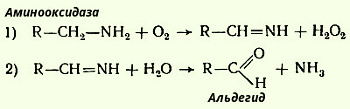
При цій реакції утворюється вільний аміак. Інактивація амінів досягається також шляхом їх зв'язування з білками.
Накопичення біогенних амінів в тканинах і крові і прояв їх токсичної дії виникають: при посиленні активності декарбоксилаз, гальмуванні активності оксидаз і порушенні зв'язування їх з білками.
Вміст біогенних амінів в тканинах і крові збільшується при гіпоксії і деструкції тканин.
При патологічних процесах, що супроводжуються пригніченням окислювального дезамінування, перетворення амінокислот в більшій мірі відбувається шляхом декарбоксилювання з накопиченням біогенних амінів.
Порушення обміну окремих амінокислот. Існує ряд спадкових захворювань людини, пов'язаних з вродженими дефектами обміну окремих амінокислот. Ці порушення обміну амінокислот пов'язані з генетично обумовленим порушенням синтезу білкових груп ферментів, які здійснюють перетворення амінокислот (див. § 57 ).
§ 189. Порушення кінцевих етапів білкового обміну
Порушення мочевінообразованія. Кінцевими продуктами розпаду амінокислот є аміак, сечовина, СO2 і Н2О. Аміак утворюється в усіх тканинах в результаті дезамінування амінокислот. Аміак токсичний, при його накопиченні пошкоджується протоплазма клітин. Для зв'язування аміаку і його знешкодження існують два механізми: в печінці утворюється сечовина, а в інших тканинах аміак приєднується до глютаминовой кислоті (амідування) - утворюється глютамин. Надалі глютамин віддає аміак для синтезу нових амінокислот, перетворення яких завершуються утворенням сечовини, що виділяється з сечею. З усього азоту сечі на частку сечовини доводиться 90% (аміаку близько 6%).
Синтез сечовини відбувається в печінці в цитрулін-аргінін-орнітіновом циклі (рис. 32). Існують захворювання, пов'язані з спадковим дефектом ферментів мочевінообразованія.
Аргінінсукцінатурія. Полягає в гіпераміноацідуріі (аргінінянтарная кислота) і в олігофренії. Причина - дефект ферменту аргінінсукцінаталіази.
Аммонійемія. У крові збільшена концентрація аміаку. Підвищено екскреція глютамина з сечею. Причина захворювання - блокування карбамілфосфатсінтетази і орнітінкарбамоілтрансферази, які каталізують зв'язування аміаку і освіту орнитина в циклі мочевінообразованія.
Цітруллінурія. Концентрація цитруллина в крові може збільшуватися понад норму в 50 разів. Із сечею виводиться до 15 г цитруллина на добу. Причина - спадковий дефект аргінінсукцінатсінтетази.
Активність ферментів синтезу сечовини порушується і при захворюваннях печінки (гепатити, застійний цироз), гіпопротеїнемія, пригніченні окисного фосфорилювання. У крові і тканинах накопичується аміак - розвивається амонійна інтоксикація.
Коли синтез сечовини виявляється порушений, великі кількості аміаку зв'язуються глютамат, в результаті чого останній виключається з обміну. При прискоренні переаминирования амінокислот з альфа-кетоглютарової кислотою вона не включається в цикл Кребса, обмежується окислення піровиноградної і оцтової кислот і вони перетворюються в кетонові тіла. Знижується споживання кисню. Розвивається коматозний стан.
Порушення обміну сечової кислоти. Подагра. Сечова кислота - кінцевий продукт обміну амінопуріна (аденін і гуанін) у людини. У рептилій і птахів сечова кислота є кінцевим продуктом обміну всіх азотистих з'єднань. У крові у людини зазвичай міститься 40 мг / л сечової кислоти. При надмірному споживанні продуктів, багатих пуриновими нуклеотидами і амінокислотами в організмі збільшується кількість сечової кислоти. Концентрація її зростає також при нефриті, лейкемиях. Виникає гіперурикемія.
Іноді гіперурикемія супроводжується відкладенням солей сечової кислоти в хрящах, сухожильних піхвах, нирках, шкірі і м'язах, так як сечова кислота погано розчинна. Навколо відкладень кристалічних уратів виникає запалення - створюється грануляційний вал, навколишній омертвілі тканини, утворюються подагричні вузли. Урикемия може супроводжуватися випаданням солей сечової кислоти в сечових шляхах з утворенням конкрементів.
Патогенез подагри не ясний. Припускають, що захворювання носить спадковий характер і пов'язане з порушенням факторів, що підтримують сечову кислоту в розчинній стані. Ці фактори пов'язані з обміном мукополісахаридів і мукопротеїдів, які утворюють центр кристалізації. При порушенні функції печінки (інтоксикація) збільшується відкладення уратів в тканинах і виділення уратів з сечею.
продовження: Глава 5. Порушення вуглеводного обміну
До змісту


