- Йога начинающим видео
- Хулахуп танец видео
- Смотреть моя тренировка видео
- Видео тренировки александра емельяненко
- Как правильно крутить обруч на бедрах видео
- Тренировки в кудо видео
- Тренировки рой джонса видео
- Йога онлайн смотреть видео
- Тренировки костя дзю видео
- Видео тренировки роя джонса
- Видео спинальной
- Айенгар йога видео
- Йога для женщин на видео
- Правильно крутить обруч видео
- Плиометрические отжимания видео
- Новости

Управление Здравоохранения Евпаторийского городского совета (С)2011
67 гостей
Medline.ru - Біомедичні журнал ОСНОВИ ТОКСИКОЛОГІЇ
ТОМ 4, СТ. 119 (стор.) // березень, 2003 р
ОСНОВИ ТОКСИКОЛОГІЇ
С. А. Куценко
Санкт-Петербург, 2002 г.
ГЛАВА 1.4. Властивості токсикантів, ЩО ВИЗНАЧАЮТЬ ТОКСИЧНІСТЬ
Токсичність різних речовин неоднакова. Оскільки вона проявляється у взаємодії ксенобиотика з біологічною системою, її величина залежить від властивостей як токсиканти, так і біосистеми і в кінцевому підсумку визначається:
1. Здатністю речовини досягти структури-мішені, взаємодія з якою ініціює токсичний процес;
2. Характером і міцністю зв'язку, що утворюється між токсикантом і структурою-мішенню;
3. Значним структури-мішені для підтримки гомеостазу в організмі.
Будова біологічних систем, особливості їх морфо-функціональної організації в значній мірі незмінні в масштабах історично недалекого часу. У зв'язку з цим, оскільки речовина має цілком певні властивості, воно надає на організм (біологічну систему) відтворений з відомим постійністю ефект. Зміна властивостей чинного фактора (вплив іншим речовиною) буде супроводжуватися якісними і / або кількісними змінами, що розвиваються ефектів. Найважливішим принципом токсикології є залежність якісних і кількісних характеристик розвивається токсичного процесу від будови діючої речовини.
Будова речовини визначає розміри молекули, її масу, розчинність, летючість, агрегатний стан при нормальних умовах і хімічну активність. Всі ці властивості впливають на токсичність речовини, в той же час, жодне з них не є єдиним важливим.
Розміри молекули токсиканти впливають на його біологічну активність в силу ряду причин:
а). Зі збільшенням молекулярної маси ускладнюється процес надходження токсиканту в організм і розподілу його в органах і тканинах.
Низькомолекулярні, інертні в хімічному відношенні речовини у вигляді газу або у формі розчину, як правило, легко проникають в кров через легені, шлунково-кишковий тракт, іноді і шкіру, швидко розподіляються в тканинах, проходячи через гістогематичні бар'єри. Однак уже для низькомолекулярних сполук здатність проникати через бар'єри в чому визначається розчинністю. Гідрофільні молекули навіть з молекулярної масою 50 - 100 Д мають обмежену здатність проникати, наприклад, через слизові оболонки.
Для високомолекулярних сполук процес проходження через бар'єрні структури, як правило, утруднений. З іншого боку ліпофільні речовини, часом, не дивлячись на великі розміри молекул, відносно легко проходять через біологічні бар'єри. Великі молекули речовин погано розчинних у воді і ліпідах (штучні і природні полімери) практично не проникають у внутрішні середовища організму і, отже, не володіють загальнийтоксичними дією.
б). Зі збільшенням молекулярної маси збільшується число можливих ізомерних форм молекули токсиканти і, одночасно, зростає специфічність їх дії.
Оскільки структури організму, що вступають у взаємодію з токсикантом, в більшості випадків мають цілком певну просторову організацію, активність діючої речовини істотно залежить від його конформації. Чим більше молекула, тим виразніше виступає ця залежність. Так, низькомолекулярні граничні вуглеводні і деякі їх похідні діють практично неспецифічно, причому, як на одноклітинні, так і на складно організовані багатоклітинні організми. Малі розміри цих молекул обумовлюють обмежену кількість їх ізомерних форм, а отже збільшують кількість ділянок їх неспецифічного зв'язування в організмі.
Зі збільшенням розмірів молекул речовин зростає число токсикантів, що мають однакову масу і близьке будову, але що володіють абсолютно різною токсичністю. Так, з більш ніж 100 ізомерів тетрахлоро-пара-дібензодіоксини, високою токсичністю володіє лише один: 2,3,7,8-тетрахлоро-пара-дібензодіоксини.
Для групи високомолекулярних речовин (полімери), однак, також досить характерно неспецифічне дію. Воно може бути обумовлено, наприклад, модифікацією колоїдно-осмотичного тиску крові.
в). Зі збільшенням розмірів молекули зростає ймовірність взаємодії токсикантів з біосубстратами за рахунок сил Ван-дер-Ваальса (див. Нижче).
Чим більше розміри молекули, тим більше число атомів токсиканти контактує з ділянкою його зв'язування, тим міцніше формується при цьому зв'язок. Оскільки великі молекули мають відому "гнучкістю", це в ще більшому ступені сприяє "притискання" лиганда до рецептора, тобто збільшення його афінності. В основному за рахунок сил Ван-дер-Ваальса нейромедіатори, гормони (і інші ендогенні біорегулятори) взаємодіють з рецепторним апаратом клітин, органів, тканин. Однак сили ці, як правило, не великі і відразу після впливу відбувається дисоціація комплексу біорегулятор-рецептор. Окремі токсиканти, що нагадують будовою ендогенні біологічно активні речовини, також вступають у взаємодію з рецепторами, імітуючи (агоністи) їх ефекти. Такий механізм лежить в основі токсичної дії багатьох алкалоїдів (нікотину, анабазіна і ін.), Глікозидів, синтетичних токсикантів і т.д. Якщо токсикант має істотно більші розміри, ніж природний агонист, то за рахунок сил Ван-дер-Ваальса здійснюється його міцна фіксація на рецепторі. Це призводить до екранування рецепторів від дії агоністів, їх блоку (антагоністи). Так діють, наприклад, атропін і курарін на, відповідно, М- і Н-холінорецептори, ДЛК - на рецептори серотоніну, і т.д. Серед токсичних речовин значно більше число є антагоністами відповідних молекул-биорегуляторов.
2. Геометрія молекули токсиканти
Хімічна формула, як правило, несе недостатньо інформації про властивості речовини, зокрема про геометрію молекули. Разом з тим вивчення залежності "будова - активність" в токсикології можливо тільки з урахуванням уявлень про просторову організацію молекул токсиканти.
Молекули речовин можуть бути ригідними і гнучкими. Ригідні молекули мають постійну просторову організацію. Це перш за все речовини, утворені циклічними радикалами, що містять полівалентні мостіковие зв'язку (алкалоїди, полігалогеновані дібензофурани, бенз (а) пірен та багато інших). Конформація "гнучких" молекул, що містять в структурі алифатические ланцюга, групи, з'єднані простими зв'язками, завжди невизначена, за рахунок постійної зміни в часі взаємного розташування радикалів. Однак і у цих речовин часом можна виділити переважну конформацію. Так, найбільш імовірна форма молекули 1,2-дихлоретан, при якій атоми хлору знаходяться в найбільшому видаленні друг від друга (транс-ізомери) (рисунок 1).
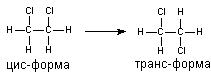
Малюнок 1. цис- і транс-форма дихлоретану
Велика кількість хімічних речовин, що відрізняються високою токсичністю, існує у формі ізомерів. Основні форми ізомерії це: структурна, оптична, геометрична, таутомерія (проблема глибоко розглядається в сучасних курсах "Загальною хімії").
У низькомолекулярних речовин, таких як дихлоретан, відмінності просторової організації ізомерів незначно позначаються на їх біологічної активності. Як уже зазначалося, такі молекули, здебільшого, викликають малоспецифичними ефекти: наприклад, порушення проникності збудливих біологічних мембран, освіта ковалентних зв'язків з молекулами білків, нуклеїнових кислот і т.д. Значні відмінності спостерігаються при дії великих молекул токсикантів, переважно взаємодіють з певним чином просторово організованими специфічними рецепторами для ендогенних біорегуляторів. Так, якщо оцінити розміри більшості відомих нейромедіаторів, то з'ясовується, що молекулярна маса більшості з них лежить в інтервалі 160 - 190 Д. Молекули ацетилхоліну та адреналіну складаються з 26 атомів, серотоніну - 25, норадреналіну - 23. Природно очікувати, що і токсиканти, взаємодіють з рецепторами цих нейромедіаторів, повинні мати близькі розміри і, отже, цілком певну просторову організацію. У цьому випадку роль ізомерії в біологічної активності речовин зростає. Аналогічні міркування стосовно токсикантів - конкурентним інгібіторів багатьох ферментів (наприклад, інгібіторів ацетилхолінестерази: фосфорорганічних сполук і карбонат). Основні закономірності, що визначають вплив ізомерії на токсичність речовин полягають у наступному:
1. Чим специфичнее взаємодія речовини і рецептора, тим виразніше відмінності в дії ізомерів. Оскільки токсичність в значній мірі визначається специфічністю взаємодії токсиканти зі структурами-мішенями, що мають велике значення в підтримці гомеостазу в організмі, можна стверджувати, що чим вище токсичність речовини, тим істотніше відмінності біологічної активності його ізомерів.
2. Якщо асиметричний атом в молекулі токсиканти займає ключову позицію, визначальну багато в чому його ефект, то відмінності в дії ізомерів, як правило, істотні. І навпаки, якщо асиметричний атом знаходиться в положенні, не визначає біологічний ефект, то стереоізомери володіють практично однаковою токсичністю.
3. Чим жорсткіше конформація рецептора, тим більш виражені відмінності активності, що діють на нього ізомерів токсиканти. Так, структурна гнучкість Н-холінорецепторів гангліонарних і нейром'язових синапсів виражена на стільки, що стереоізомери речовин, що взаємодіють з ними, мають практично однаковою активністю.
Відмінності в токсичності стереоизомеров можуть бути пов'язані не тільки з особливостями їх токсікодінамікі, але і токсікокінетікі (активний транспорт через мембрани, метаболізм). Так, алкалоїд L-скополамін швидко руйнується естераз плазми крові кролика на L-Тропова кислоту і Тропін (Скопин), втрачаючи біологічну активність. D-скополамін не руйнується ензимом і тому діє значно довше.
3. Фізико-хімічні властивості речовини
Фізико-хімічні властивості речовин істотно позначаються на їх токсичності. Визначальними є: розчинність в воді, розчинність в ліпідах, кислотно-основна природа токсиканти.
А. Розчинність в воді.
Розчинність токсиканти в воді - необхідна умова його розробці у внутрішні середовища організму: corpora non agunt nisi soluta (що не розчиняється, то не діє). Для того, щоб досягти структури-мішені токсикант також повинен потрапити в водну фазу, так як вода - основа міжклітинної рідини організму. Полярність молекули води вимагає і від токсиканта відомої полярності. Тому розчинність речовини у воді залежить від наявності та кількості в його молекулі полярних груп і їх будови (таблиця 1).
Таблиця 1. Розчинність деяких похідних бензолу у воді (г / 100г С300)
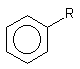
R
-C2H5
-J
-Br
-Cl
-CH3
-F
-NO2
-SO3H
г / 100г
води
не розчин.
0,034
0,045
0,049
0,057
0,15
0,19
розчин.
Деякі речовини виявляють властивості кислот або підстав і, отже, можуть перебувати в розчині в протоновану або депротонованої формі. Це також позначається на їх розчинності (малюнок 2).
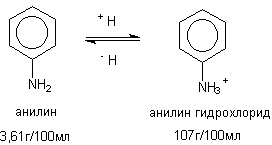
Малюнок 2. Розчинність аніліну і його протоновану похідного
Як видно з наведеного рисунка, наявність заряду в молекулі токсиканти істотно позначається на його здатності розчинятися у воді, посилюючи диполь-диполь взаємодію розчинника і розчиненої сполуки.
Б. Розчинність в ліпідах.
Розчинність в ліпідах має основне значення для процесів проникнення і розподілу великих молекул токсикантів в організмі. Крім того, чим вище розчинність речовини в ліпідах, тим гірше воно виводиться з організму. Мірою жиро-розчинності токсикантів є кількість речовини, здатна до розчинення в одиниці об'єму рідких масел або органічних розчинників. При аналізі отриманих результатів слід мати на увазі, що в різних розчинниках речовина розчиняється по-різному. Так, розчинність амидопирина (г / 100г 370С) в бензолі становить 0,81; в топленому салі - 1,7; олії - 2,0; суміші бензолу і лецитину (1: 1) - 12,6; хлороформі - 120,6.
Нерозчинні в жирах молекули можуть потрапити в організм з навколишнього середовища лише в тому випадку, якщо вони проходять через пори біологічних мембран, або переносяться через бар'єри за допомогою спеціальних механізмів, наприклад, пиноцитоза і т.д. (Див. Розділ "Токсікокінетіка").
Великі, нерозчинні в ліпідах речовини, як правило, відносяться до числа малотоксичних.
Жиророзчинні і водорастворимость - пов'язані між собою властивості. Чим полярних молекул речовини, тим краще вона розчиняється в воді і гірше - в ліпідах. Найбільшою біологічною активністю, як правило, мають токсиканти з проміжною розчинністю. У зв'язку з цим важливою для токсикології характеристикою є коефіцієнт розподілу речовини в середовищах: масло / вода або гептан / вода. Для деяких речовин їх біологічна активність пропорційна величині цього коефіцієнта (таблиця 2)
Таблиця 2. Залежність токсичності аліфатичних спиртів від їх жиро-і водорозчинності *.
параметри
СН3ОН
С2Н5ОН
С3Н7ОН
С4Н9ОН
С5Н11ОН
С6Н13ОН
С8Н17ОН
ЛД50 в / в (мМ / кг)
миші
177
53,7
18,2
5,09
2,09
1,01
0,53
гемоліз еритроцитів
кролика (М)
7,43
4,11
0,80
0,44
0,18
0,06
0,02
Пригнічення активності каталази на 50% (М)
3,6
3,47
2,36
1,95
1,33
-
-
* - жиророзчинні збільшується зі збільшенням молекулярної маси спирту.
Чітку кореляцію можна простежити лише в гомологічних рядах токсикантів, при цьому оцінюються ефекти, як правило, неспецифічні (денатурація ензиму, порушення властивостей біологічних мембран, наркоз, пошкодження клітини, смерть).
Для специфічної взаємодії токсиканти зі структурою-мішенню розчинність в воді або ліпідах має невпорядковане значення.
В. Кислотно-основна природа токсиканти.
Численні токсиканти є слабкими кислотами або підставами, тобто можуть, в залежності від рН середовища, перебувати в протоновану або депротонованої формі. Кислоти, перебуваючи в протоновану формі - незаряджені молекули, азотисті основи, навпаки, являють собою катіони. У депротонованої формі кислоти являють собою аніони, а підстави - не заряджені. Сила кислоти або підстави визначається здатністю до дисоціації, яка характеризується величиною константи дисоціації (Ка або рКа - негативний десятковий логарифм значення Ка). Чим вище значення рКа, тим легше здійснюється процес протонирования речовини. Підстави з високим значенням рКа - більш серйозна причина; кислота з високим рКа - слабка кислота. Так, диметиламин (рКа 10,7) - більш серйозна причина, чому N-метиланилин (рКа 4,7); фенол (карболова кислота рКа 9,9) - більш слабка кислота, ніж бензойна кислота (рКа 4,2). Співвідношення іонізованої і неионизированной форм токсикантів в середовищі крім величини рКа, визначається рН середовища. Зі збільшенням рН збільшується число незаряджених молекул підстав і заряджених аніонів кислот.
Часто іонізація токсиканти супроводжується посиленням його спорідненості до рецептора, проте одночасно ускладнюється проходження молекули через біологічні бар'єри.
Сильні кислоти і луги (повністю диссоциирующие у водних розчинах), при дії на тканини організму, різко змінюючи рН, викликають денатурацію макромолекул клітин. Цей процес лежить в основі хімічного опіку покривних тканин.
Біологічна дія токсикант може надавати лише за умови його достатньої стабільності в навколишньому середовищі і середовищах організму. Якщо речовина нестабільно, то розвивається ефект пов'язаний з впливом продуктів його перетворення. Активні в хімічному відношенні речовини рідко стають безпосередніми причинами загальнотоксичної дії. Ці речовини, або вже в навколишньому середовищі вступають в хімічні реакції, перетворюючись в більш інертні, але відносно стабільні з'єднання, або реагують з покривними тканинами організму (шкірою, слизовими), витрачаючи свій хімічний потенціал на їх альтерацию (місцеву дію).
Після потрапляння в організм більша частина ксенобіотиків з різною швидкістю піддаєтьсябіотрансформації. Так, при надходженні в шлунково-кишковий тракт пептиди і білкові молекули (наприклад, тетанотоксін) швидко інактивуються пептидазами і протеиназами. У процесі руйнування токсикантів різної будови бере участь і кишкова флора. Метаболізм ксенобіотиків завершується в крові і тканинах після їх розробці. Тому, часом, дуже важко вирішити, яка саме речовина є безпосередньо діючим початком розвивається токсичного процесу.
Взаємодія токсиканти з молекулами-мішенями організму підкоряється тим же закономірностям, що і будь-яка інша хімічна реакція, що протікає ex vivo і, отже, багато в чому залежить від його хімічних властивостей.
Більшість високо цієї токсичної сполуки - інертні в хімічному відношенні молекули. Сила міжмолекулярної взаємодії між токсикантом і біологічної молекулою-мішенню діє, як правило, локально; утворюється зв'язок здатна до дисоціації. Вивільнена з зв'язку з токсикантом біомішені відновлює вихідні властивості. У подібних випадках досить елімінувати не пов'язаної частина токсиканти з організму для того, щоб зрушити хімічну рівновагу в бік руйнування комплексу токсикант-мішень, і, тим самим, усунути дію отрути.
Іноді між токсикантом і молекулою-мішенню утворюються міцні зв'язки. У цих випадках зруйнувати комплекс токсикант-біомішені часом можливо тільки за допомогою інших засобів, що утворюють з отрутою ще більш міцні комплекси. Зокрема, для відновлення активності ацетилхолінестерази, ингибированной фосфорорганічними сполуками (ФОС), застосовують речовини з групи оксимов, що вступають у взаємодію з токсикантами і викликають тим самим дефосфорілірованіе активного центру ензиму.
5.1. Типи хімічних зв'язків, що утворюються між токсикантами і молекулами-мішенями організму
При взаємодії токсиканти з біологічними структурами-мішенями можуть утворюватися різні типи хімічних зв'язків (таблиця 3).
Таблиця 3. різні типи зв'язків, що формуються між токсикантами і молекулами-мішенями організму
вид зв'язку
приклад
енергія зв'язку
(кДж / мол)
іонна
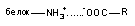
20
ковалентний
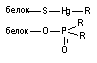
40 - 600
Донорно-акцепторная
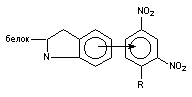
4 - 20
Іон-дипольна

8 - 20
Диполь-дипольна
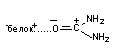
4 - 12
воднева

4 - 28
Ван-дер-Ваальса
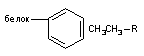
1 - 4
гідрофобна

1 - 6
Іонна зв'язок. У водних розчинах багато речовини дисоціюють з утворенням іонів. Між позитивно і негативно зарядженими іонами токсиканти і ендогенними іонами-мішенями починають діяти сили електростатичного притягання. Внаслідок тяжіння виникає хімічний зв'язок. Зв'язок такого типу називається електровалентной або іонної. Освічені катіонами і аніонами речовини не несуть електричного заряду.
А- + В +  АВ
АВ
Токсичні наслідки подібної взаємодії в організмі розвиваються в разі утворення не розчинної у воді комплексу іона-токсиканти з біологічно значимим іоном-мішенню. Наприклад, при інтоксикації фторидами, іон фтору може вступати у взаємодію з іоном кальцію. В результаті утворюється нерозчинний фторид кальцію. Розвивається гипокальциемия має певне значення для розвитку і прояви інтоксикації. Аналогічним чином діє щавлева кислота, що утворюється в організмі в процесі метаболізму етиленгліколю при інтоксикації останнім:
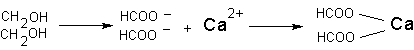
Оскільки ступінь дисоціації багатьох речовин у водному розчині істотно залежить від рН середовища, кількість які утворилися за рахунок іонної зв'язку комплексів токсикант-мішень також залежить від цього показника.
Ковалентний зв'язок. Для утворення ковалентного зв'язку, взаємодіючі атоми повинні мати на зовнішній електронній орбіті неспарені електрони. Ці електрони займають одну і ту ж орбіталь, а що утворилася загальна пара формує силу тяжіння між атомами. В результаті утворення такої загальної пари електронів кожен з взаємодіючих атомів набуває "завершений набір" електронів і утворене з'єднання стає стабільним. Енергія ковалентного зв'язку велика і становить 200 - 400 кДж / мол
Висока стабільність зв'язку цього типу означає практично незворотного характеру приєднання токсиканти до структури-мішені. Прикладами речовин, що утворюють з биомолекулами подібний зв'язок, є ФОС (взаємодіють з серином, що входять в структуру активного центру ацетилхолінестерази), іприт (взаємодіють з пуриновими підставами нуклеіенових кислот), а також цілий ряд інших поширених токсикантів (метилбромід, метилхлорид, етиленоксид і ін. ). Внаслідок міцності утворилася зв'язку, руйнування комплексу токсикант-біомішені можливо тільки за допомогою спеціальних засобів (наприклад, реактіваторов ХЕ при інтоксикації ФОС). Заповнення змісту пошкодженої токсикантом біологічної структури можливо також за рахунок синтезу її de novo. Так, відновлення активності АХЕ в тканинах лабораторних тварин отруєних зоманом проходить зі швидкістю синтезу ензиму нервовими клітинами.
Координаційна зв'язок - це ковалентний зв'язок, в якій усуспільнення пару електронів надає тільки один з беруть участь в зв'язку атомів. Один з атомів є донором, а інший акцептором електронної пари, тому цей зв'язок називають також донорно-акцепторної. Акцепторами часто є катіони металів, або атоми перехідних металів (Zn, Cu, Fe), що входять до складу молекули. Таким чином, зокрема, оксид вуглецю взаємодіє з залізом гемоглобіну, з освіту карбоксигемоглобина.
Водневий зв'язок. Ковалентний зв'язок між атомом водню і електронегативний атомом (кисень, азот, сірка і т.д.) більш-менш поляризована
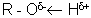
Внаслідок цього атом водню набуває незначний позитивний заряд. Якщо поблизу такого атома знаходиться молекула або група, що містить аніон або електронегативний атом, між ними утворюється слабкий зв'язок, звана водневої.
Воднева зв'язок може утворюватися як між молекулами, так і між атомами всередині молекул. Енергія зв'язку не велика і в водному розчині становить близько 20 кДж / мол. Її міцність багато в чому залежить від будови взаємодіючих речовин, зокрема, від ступеня електронегативності атомів, пов'язаних з воднем. Електронегативність атомів зростає в ряду:
Н = P <C = S = I <Br <Cl = N <O <F
2,1 2,1 2,5 2,5 2,5 2,8 3,0 3,0 3,4 4,0
Водневі зв'язки мають дуже велике значення для підтримки просторової структури білків, нуклеїнових кислот та інших високомолекулярних сполук. Речовини, здатні руйнувати водневу зв'язок, можуть порушувати просторову структуру макромолекул (явище інтерколаціі: вбудовування молекул акридину, етідіумброміда між площинами, утвореними витками спіралі молекули ДНК).
До складу молекул токсикантів також входять групи, здатні брати участь в утворенні водневих зв'язків. Якщо ці групи (Х-Н) є структурними елементами "активного" радикала токсиканти, то вони беруть участь в утворенні складної зв'язку речовини з молекулою-мішенню. Оскільки водневі зв'язки є по суті електростатичними, їх сила слабшає в присутності речовин, що володіють властивостями діелектриків ( "неелектролітів").
Зв'язки Ван-дер-Ваальса. Форма електронної хмари молекул квазістабільності, тобто не змінюється до тих пір, поки на неї не діють зовнішні сили. Під впливом електромагнітних полів електронні хмари молекул деформуються. При цьому байдуже викликано поява деформіруящіх сил впливом зовнішніх полів або поле сформовано прилеглими іонами, диполями, аполярних молекулами. Ступінь деформированности електронної хмари залежить від енергетичних характеристик впливають полів і поляризуемости самої молекули. Здатність електронного хмари до деформації (поляризованість) залежить від розмірів молекули. У великих молекул вона більше, ніж у малих, оскільки змістити електрони, що знаходяться на значній відстані від ядра атома, легше.
Деформуюче вплив полів перетворює неполярні молекули в диполі, так як центри максимальної щільності позитивного і негативного зарядів молекули кілька роз'єднуються в просторі. Сформувався диполь називають індукованим або тимчасовим, оскільки він перестає існувати відразу після припинення дії деформуючих сил. Дві сусідні неполярні молекули можуть взаємно індукувати утворення тимчасових диполів і, таким чином взаємодіяти один з одним. Сили взаємодії, що формуються між тимчасовими диполями, називаються силами Лондона - Ван-дер-Ваальса. Енергія утворюється зв'язку мала, проте вона істотно зростає при збільшенні числа ділянок контакту між взаємодіючими молекулами. З боку токсиканти це можуть бути ароматичні, гетероциклічні алкільні радикали; з боку рецептора - неполярні ділянки молекул амінокислот (лейцин, валін, аланін, пролін і ін.). Внесок кожної -СН2- групи алкільного ланцюга у взаємодію оцінюється в 2 - 4 кдж / мовляв. При тісному контакті великих неполярних молекул енергія зв'язку може досягти дуже великих величин. Тому при утворенні комплексу токсикант-біомішені сили Ван-дер-Ваальса можуть забезпечувати дуже міцну фіксацію ксенобиотика. Діюча сила, відповідальна за формування зв'язку, обернено пропорційна сьомий ступеня відстані між молекулами. Тому вона не може забезпечити тяжіння молекул токсиканти, вільно циркулюють в середовищі, до рецептора. У цьому процесі першорядну роль грають сили електростатичного взаємодії. Однак після того як контакт між токсикантом і рецептором здійснився сили Ван-дер-Ваальса забезпечують його орієнтацію і щільну фіксацію.
Гідрофобна взаємодія. Гідрофобні зв'язку формуються у водному середовищі, коли молекули взаємодіють речовин контактують один з одним неполярними (гідрофобними) ділянками. На відміну від взаємодії Ван-дер-Ваальса і донорно-акцепторної взаємодії, які також формуються при взаємодії неполярних груп, освіта гідрофобних зв'язків обумовлено властивостями води, без участі якої взаємодія відбуватися не може. Відповідно до теорії, молекули води пов'язані один з одним водневими зв'язками, утворюючи тривимірну структуру (кластер), що нагадує структуру льоду. На кордоні поверхні, що розділяє неполярну молекулу і молекули води, утворення такої структури може. При контакті двох неполярних молекул, розчинених у воді, загальна площа поверхні, що розділяє воду і ці молекули зменшується. Внаслідок цього, мобілізується частина молекул води, організованих в кластер. На противагу всім іншим хімічним зв'язкам і взаємодій гидрофобная зв'язок, таким чином, обумовлена перетворенням розчинника (води), а не розчинених взаємодіючих речовин. Рушійною силою освіти зв'язку є зростання ентропії цілісної системи розчинник - розчинені молекули. Структурна організація гідрофобних, взаємодіючих молекул зростає (зменшення ентропії), але при цьому істотно дезорганизуется (ентропія зростає) структура розчинника (води).
Гідрофобні зв'язку мають велике значення при взаємодії неполярних молекул ксенобіотиків з клітинними і внутрішньоклітинними мембранами, для освіти їх комплексів з білками, при цьому можливе порушення конформації макромолекул.
В процесі взаємодії низькомолекулярної речовини з біомішені практично завжди формується кілька типів зв'язків (рисунок 3), оскільки молекула токсиканти, як правило, включає полярний (іноді навіть іонізований), і неполярний фрагменти.
Іонні зв'язку, за рахунок яких здійснюється тяжіння молекули до біомішені, мало специфічні (аналогічно іон-дипольному і диполь-дипольному взаємодії). Взаємодія між неполярними групами також неспецифічно. Однак, якщо в структурі мішені (наприклад, рецепторі для ендогенних біорегуляторів) полярні і неполярні групи просторово організовані, між цими ділянками і особливими ділянками молекули токсиканти утворюються специфічні зв'язки, обумовлені просторовою організацією молекули токсиканти. Така взаємодія можна порівняти з орієнтацією намагнічених стрілок в магнітному полі. Після орієнтації молекули за допомогою іонного (диполь-дипольного) взаємодії між нею і рецептором формується тісний контакт, і утворюються зв'язку за рахунок водневих сил і сил Ван-дер-Ваальса. Утворений комплекс тим більш міцний, ніж більш комплементарна молекула токсиканти рецептора.


