- Йога начинающим видео
- Хулахуп танец видео
- Смотреть моя тренировка видео
- Видео тренировки александра емельяненко
- Как правильно крутить обруч на бедрах видео
- Тренировки в кудо видео
- Тренировки рой джонса видео
- Йога онлайн смотреть видео
- Тренировки костя дзю видео
- Видео тренировки роя джонса
- Видео спинальной
- Айенгар йога видео
- Йога для женщин на видео
- Правильно крутить обруч видео
- Плиометрические отжимания видео
- Новости

Управление Здравоохранения Евпаторийского городского совета (С)2011
67 гостей
Necropsy-based Wild Fish Health Assessment
Описані тут методи були схвалені Leetown науковий центр інституційний догляд тварин і використання Комітетом.
1. риба колекція
- Зберіть живої риби з мінімальним стресом. Використання човна або рюкзак електролов, гак і лінії або мереж.
- Утримуйте рибу в живій свердловин або пористий контейнерів до вибірки.
Примітка: Американське суспільство рибальства опублікував ряд посібників для риб збору, обробки і анестезії / евтаназіі26,27,28. Одягайте рукавички при обробці риби.
2. риба патанатомія
- Приспати риби.
- Місце риби в анестезії, до тих пір, поки opercular рух припиняється і риба втрачає рівновагу. Після ще 2 - 10 хв риба буде бути euthanized; Однак це також залежить від виду.
Примітка: Риба може бути euthanized ряду анестетиків (див. Таблицю матеріали для найбільш часто використовуваних). Метод евтаназія буде залежати від лабораторних вимірювань, які будуть проводитися на тканинах собрани29.
- Місце риби в анестезії, до тих пір, поки opercular рух припиняється і риба втрачає рівновагу. Після ще 2 - 10 хв риба буде бути euthanized; Однак це також залежить від виду.
- Міра біометричних характеристик.
- Вага риби до найближчого грама.
- Виміряйте довжину риби до найближчого міліметра.
- Міра Загальна довжина від кінчика рила з рот закритий до кінця хвоста спільно стискається.
- Виміряйте вилка довжина від вилки в хвіст на кінчику морда і Стандартна довжина від кінчика рила до кінця тіла (початок хвіст).
- Розрахуйте коефіцієнт за такою формулою:
Коефіцієнт = (вага всього тіла - вага гонад) / Загальна дліна3.
Примітка: Вага гонад віднімається з загальної ваги тіла так як гонад можуть істотно сприяти вага всього тіла, особливо в prespawn жінка риби.
- Отримайте зразок крові.
Примітка: Крові найчастіше беруться з хвостового вен, але може також бути виведені з спинний аорти або по серцевої прокол30.- Витягти зразок периферичної крові з хвостового вен голкою 22 або 23 G на 1-5 мл шприц, в залежності від розміру риби. Вставте голку передували хвостового області нижче бічної лінії (рис. 1A і 1B). Кут його вгору до ураження хребта і потім зняти трохи. Вен черевної вищележачі хребта.
Примітка: Якщо ви плануєте зробити мазків крові або сироватки не потрібно, використовується не антикоагулянту. У більшості випадків буде збір плазми і, отже, антикоагулянт гепарин натрію, ЕДТА або літій використовується для покриття голок і шприців і також в пробірки (наприклад, vacutainer). - Видаліть голку і помістіть в контейнер утилізації Шарпс до здачі крові в колекції трубку.
Примітка: Кров може проводитися на льоду, але завісящ на наступні аналізи слід якомога швидше, як возможних30центріфугіруют. - Якщо буде оцінюватися ядерної аномалії або диференціального крові, відразу ж місце краплі крові на ковзаннях мікроскопа дублювати чисте скло. Назад в падіння, який потім звертається по всій поверхні капілярність другий слайд під кутом 45 °. Дозвольте висохнуть31.
- Центрифуга крові в 1500 - 2500 x g 15 хв відкладеннях клітини. Видалення плазми / сироватка з стерильних передачі піпетки, аліквотах в кріогенних флаконів і зберігати при температурі-80 ° C.
- Витягти зразок периферичної крові з хвостового вен голкою 22 або 23 G на 1-5 мл шприц, в залежності від розміру риби. Вставте голку передували хвостового області нижче бічної лінії (рис. 1A і 1B). Кут його вгору до ураження хребта і потім зняти трохи. Вен черевної вищележачі хребта.

Малюнок 1: Отримання крові з риби. (A) A недавно вбиті риби укладається на його стороні і бічної лінії розташовані. (B) голчастий - вставленої вентральний до бічної лінії (стрілка), під кутом вгору до тих пір, поки голка торкнеться хребта. Потім злегка знімається, і всмоктування для вивести крові. Будь ласка, натисніть тут, щоб подивитися велику версію цієї фігури.
- Провести оцінку на основі патанатомія здоров'я на кожній риби.
Примітка: Кількість публікацій, ілюстрації і опису пошкоджень і аномалії, доступни32,33,34,35.- Документ зовнішніх відхилень, включаючи пошкодження на поверхні тіла і плавників (рис. 2), очі і зябра (рис. 3), зовнішніх паразитів, таких як п'явками (Малюнок 2D), личинки або Трематодние metacercarial кісти (Малюнок 2D, 3B) і Джилл паразитів (рис. 3D). Документ типу, розташування і розмір спостерігаються аномалії на аркушах даних, а також як фотографічно, якщо це можливо.
- Відкрийте за допомогою ножиці різання від анальної області кришечки і видаляючи шматок м'язів піддавати внутрішні органи черевної порожнини (рис. 4A).
Примітка: Якщо передня нирки будуть зібрані для імунної функції (див. Крок 5 нижче) або зразки, зібрані для бактеріологічних досліджень або вірусології, поверхні зовнішнього тіла повинні бути продезінфіковані з 70% спирту і ці проби повинні бути отримані до розкриття. Якщо тканини використовуються тільки для візуальних спостережень, аналізу плазми і гістопатології стерилізації не є необхідним. - Документ внутрішньої аномалії (рис. 4) включає загальні або фокуса знебарвлення різних органів (рис. 4B склад), наявність порушені райони (Малюнок 4E), кісти, паразитів і розмір (аномалії розширено, атрофувалися).

Малюнок 2: Приклади видимих уражень спостерігається на поверхні тіла і плавників риб. (A) A маленький, злегка еродованих поразки (стрілка) на поверхні бічних тіла. (B) A великий почервонілі області (стрілка) за участю поверхні хвостового тіла. (C) піднято, чорний поразки (стрілки) на поверхні тіла і плавників. (D) п'явок (біла стрілка) і маленькі чорні плями (чорні стрілки) на ребра. Шкали бар = 3 mm. (E) A піднято, ураження (стрілка) рослини, блідо на поверхні тіла. Будь ласка, натисніть тут, щоб подивитися велику версію цієї фігури.
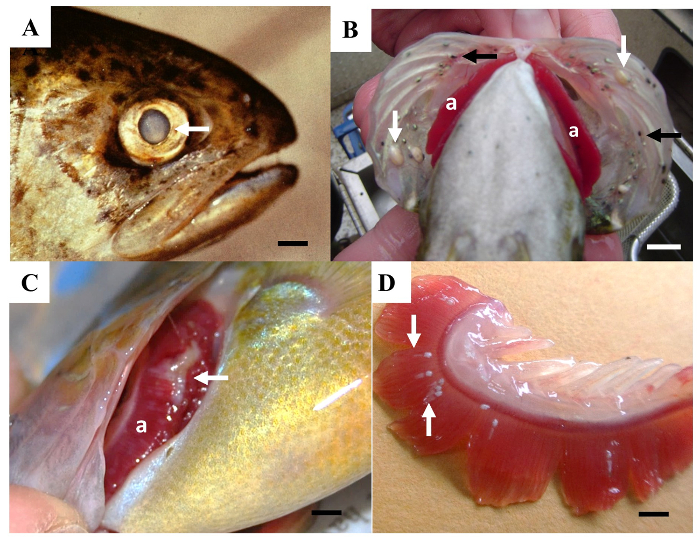
Малюнок 3: Приклади видимих пошкоджень зябра і очі риб. (A) A блідо-області (стрілка) в кришталику ока. Шкали бар = 5 mm. (B) білі кісти (білі стрілки) і маленькі чорні плями (чорні стрілки), викликані Трематодние паразитів на кришечки, що охоплюють зябра (). Шкали бар = 1 cm. (C) A блідий, ерозії в області (стрілка) на Гілл (). Шкали бар = 5 mm. (D) Гілл, яка була видалена показані паразитів (стрілки) надає Гілл ниток. Шкали бар = 2 mm. будь ласка, натисніть тут, щоб подивитися велику версію цієї фігури.
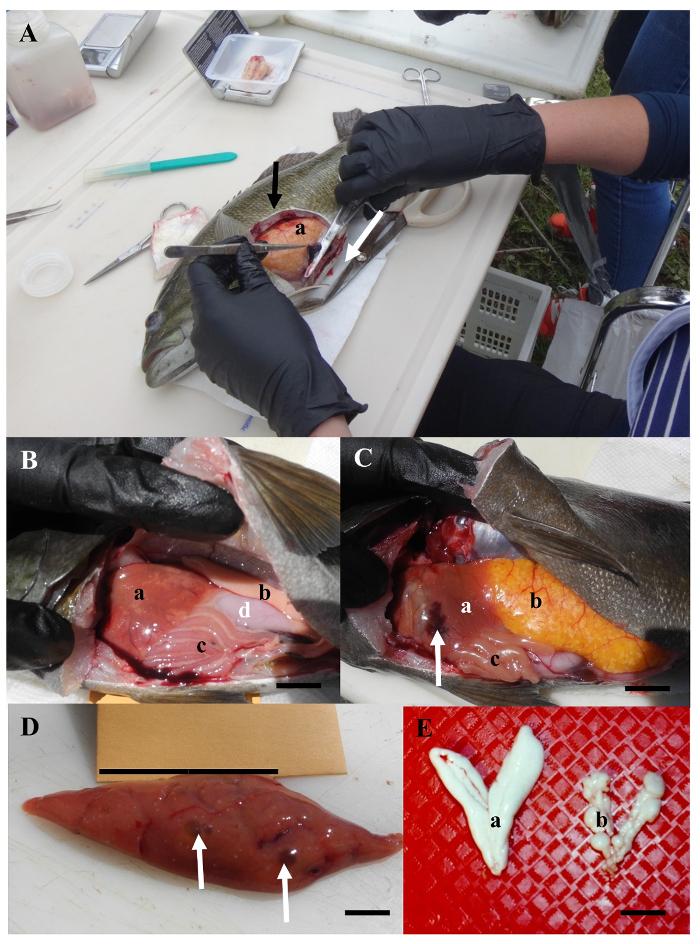
Малюнок 4: Приклади патанатомія і внутрішніх аномалій риб. (A) під час патанатомія є розрізати рибу (уздовж білої стрілкою) і клапоть м'язів (чорна стрілка) видалені, щоб викрити гонад () і селезінки, утримуються щипцями і ножиці. (B) строкаті печінки (), насінників (b), шлунково-кишкового тракту, оточений жирової жиру (c) і шлунка (d). Шкали бар = 5 mm. (C) печінки (а) з темно червона площа (стрілка), яєчників (b) і кишечника (c). Шкали бар = 5 mm. (D) печінки з зеленуватим знебарвленими областях (стрілки). Шкали бар = 1 cm. (E) приклад звичайного () і аномальні яєчок (b) з підняті конкрецій. Шкали бар = 1 cm. будь ласка, натисніть тут, щоб подивитися велику версію цієї фігури.
- Отримайте hepatosomatic індекс (HSI).
- Видаліть печінку, розірвавши печінкової артерії і сполучної тканини переднього кінця. Обережно вийміть під час обрізки спайок та інші сполуки в кишечнику і жирової жиру. Подбайте, щоб не пробивайте жовчного міхура. Вага печінки.
Примітка: Деякі риби, наприклад, коропові, не мають дискретні печінки, але швидше за печінкової тканини, загорнуті навколо кишечника та інших органів. Для цих видів він не може бути можливо отримати печінки ваг. - Розрахуйте hepatosomatic індекс (HSI) за формулою:
HSI = маса печінки вага / всього тіла
- Видаліть печінку, розірвавши печінкової артерії і сполучної тканини переднього кінця. Обережно вийміть під час обрізки спайок та інші сполуки в кишечнику і жирової жиру. Подбайте, щоб не пробивайте жовчного міхура. Вага печінки.
- Розрахуйте індекс gonadosomatic.
- Видалення гонади і зважити його.
- Розрахуйте gonadosomatic індекс (GSI) за формулою:
GSI = маса тіла вага / всього гонад
3. зберегти тканини для мікроскопічних патології
Примітка: Кількість фіксатори, включаючи нейтральних буферизації формаліну 10% і Z-fix, на основі формалін фіксатором з цинком, може використовуватися для збереження тканини в області. Останній є кращим, якщо такі методи, як в situ гібридизація або плямувати флуоресцентні антитіла можуть бути використані.
- Ретельно вирізати, але не витягнути зразки тканин. Тримайте тканини окремих частин
- Місце шматків будь-яких зовнішніх відхилень в контейнері фіксують. Крім того включати суміжні частиною нормальної тканини.
Примітка: Неправильна обробка наприклад, стиснення або інші механічні пошкодження, тривалого впливу повітря або сонячного світла і заморожування може стати причиною перешкод. - Скоротити щонайменше п'ять 3-4 мм товсті шматки печінки з різних регіонів і місце в фіксують контейнер. Увімкніть нормальних і ненормальних областях, якщо спостерігається.
- Залежно від розміру помістіть весь гонад або з декількох частин уздовж однієї гонад в фіксують контейнер.
- Місце в контейнері фіксують або цілі органи, якщо малі, або шматки всі інші органи (селезінка, передній і задній нирок, зябра, серця, кишечника і шлунка). Якщо спостерігаються атипія тканин, зберегти прилеглих частиною нормальної тканини також.
4. Видаліть отоліти для аналізу віку
Примітка: Вік може бути важливою змінною в риб хвороби / риба медичних досліджень. Хоча ряд структур, включаючи ваги і колючки, були використані для визначення віку, більшість досліджень, порівняння структур знайшли отоліти дати кращі результати36,37. Костистих риб мають три пари отоліти - lapillus, sagitta і Астеріскус. Як правило отоліти сагітальній або lapillus збираються для старіння, хоча це може варіюватися від видів. Методи видалення і старіння були раніше опісанних38.
- Прорізати перешийок Гілл і зігнути голову назад. Смуги від м'язової та сполучної тканини навколо нижньої частини округлий знайти prootic булли, підняв кістляві області.
- Оцінка або вирізати з кісток різців і тріщини піддавати отоліти. Їх можна побачити неозброєним оком.
- Місце отоліти в маркованих флакона або монета конверт і зберігати при кімнатній температурі до тих пір, поки аналізуються для віку шляхом підрахунку кільця або пріращеній38. Якщо розміщення в флаконі, відкрийте кришку, коли повернувся в лабораторію і дозволяють ретельно висушіть перед зберіганням.
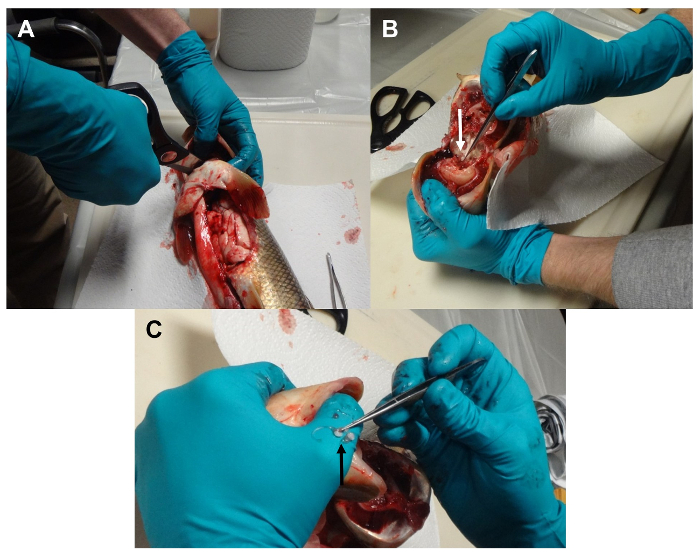
Малюнок 5: Видалення отоліти. (A) ріжеться перешийка і сполучної тканини і м'язи витягуються геть піддавати основи хребта і neurospinal області. (B) кістки тріщини піддавати отоліти. (C) Lapillar отоліти видаляються. Будь ласка, натисніть тут, щоб подивитися велику версію цієї фігури.
5. отримати тканини для аналізів імунну функцію
Примітка: Передньої нирок основних гемопоетичних органу, джерело з лімфоцитів і макрофагів функціональних аналізів і повинні бути видалені асептически, якщо буде культивованих клітин для функціональних аналізів, наприклад mitogenesis, фагоцитарної і вбивство здатності макрофагі39,40.
- Спрей зовнішньої поверхні риби з 70% етиловому спирті. Використовуйте стерильними ножицями, скальпель і щипці для відкриття черевної порожнини і видалення передньої ниркової тканини, яка темно червоний орган, розташований попереду плавальний міхур.
- Помістіть зразок передньої нирок в засобах масової інформації (наприклад, Лейбовіц L-15) щоб зберегти клітини живих. Однорідний нирок зразки з подрібнювачем стерильні ручних тканин (наприклад, Tenbroeck тканини м'ясорубку) в одну клітинку суспензій. Тримайте на мокрий лід, поки не повернувся в лабораторію.
6. зберегти тканини для аналізу нуклеїнових кислот
Примітка: Якщо течією молекулярний аналіз буде проводитися, наприклад експресії генів за допомогою Стенограма ізобіліе41 або кількісного PCR42 (полімеразна ланцюгова реакція), помістіть шматочки тканини слід оцінювати у відповідній консервант (наприклад, RNAlater стабілізації рішення) якомога швидше.
- Для збереження РНК місце два-три маленьких (2 - 3 мм) штук до відповідних консерванту в співвідношенні 10: 1 консервант обсягу тканин.
Примітка: Зразки повинні бути захищені від сонячного світла або надлишкового тепла і перевозяться на мокрий лід. - Для збереження ДНК місце два-три невеликі шматочки тканини в 95% етанолі (10: 1 етанолу тканини за обсягом). Потім, утримуючи зразки на мокрий лід і потім зберігати при температурі від-20 ° C.


