- Йога начинающим видео
- Хулахуп танец видео
- Смотреть моя тренировка видео
- Видео тренировки александра емельяненко
- Как правильно крутить обруч на бедрах видео
- Тренировки в кудо видео
- Тренировки рой джонса видео
- Йога онлайн смотреть видео
- Тренировки костя дзю видео
- Видео тренировки роя джонса
- Видео спинальной
- Айенгар йога видео
- Йога для женщин на видео
- Правильно крутить обруч видео
- Плиометрические отжимания видео
- Новости

Управление Здравоохранения Евпаторийского городского совета (С)2011
67 гостей
Establishment of a Clinic-based Biorepository
Наскільки відомо автору, цей протокол є першим у своєму роді, який фокусується на клінічних закупівлі зразків шкірних тканин як з точки зору витрат, так і з швидким підходом. Пацієнти, які проходять мікрохірургію Мооса, як правило, призначаються в певні періоди часу, і їх збір обмежується цими періодами. Збір зразків включає в себе зусилля медичного асистента, залученого в лікування пацієнтів, гістонолога Мооса, який обробляє зразки пухлини, і призначеного співробітника лабораторії, який обробляє проби і обробляє кров.
Ретельна координація між трьома членами колекторської групи (тобто медичним асистентом, гістонозом Мооса і лаборантом), ми виявили, що існуючий медичний асистуючий персонал може виконати додаткові завдання, пов'язані з збором 3-5 зразків тканин У день без будь-яких видимих відстрочок в клінічних операціях. Отримання згоди пацієнта І збір букальний мазків і крові повинен бути завершений протягом звичайних періодів очікування, пов'язаних з процедурою мікрохірургії Мооса. Крім ухвалення рішення про те, як зразок повинен бути оброблений, завдання, за які відповідає гістонолог Мооса, завершуються в кінці обробки Mohs зразків пацієнтів і, як правило, додають приблизно 30 хв до щоденного графіку. Як правило, один із співробітників клініки несе відповідальність за маркування і обробку зразків крові і за будь-яку передачу і введення зразків в базу даних. Залежно від кількості оброблених зразків ці обов'язки можуть зажадати значного часу від існуючих обов'язків; Таким чином, збір зразків повинен проводитися тільки тоді, коли є достатня кількість персоналу лабораторії. Зокрема, якщо протягом одного дня буде зібрано понад 5 проб або якщо у пацієнтів буде зібрано кілька проб крові, буде потрібно кілька годин додаткових зусиль з боку лаборанта.
Jove_content "> У дні збору медичні помічники (MA) отримують згоду пацієнтів на пожертвування тканей.Матеріал згодом отримує щоковий тампон (і слину, якщо необхідно) і збирає кров для обробки лабораторним персоналом. Пацієнт після збору цих зразків, тому з точки зору пацієнта, решта відвідування клініки залишається незмінною (хоча їх просять здавати кров під час будь-якого подальшого візиту). В даний час ми можемо оцінити, що 70% пацієнтів згодні Пожертвувати тканини, причому ~ 30% цих пацієнтів також здавали кров , 30% відмовляються від участі. В даний час тільки пацієнти з підтвердженою біопсією діагностикою раку включаються в біоресурси. Пацієнти з відомим переданим кров'ю інфекційним захворюванням виключаються,
Співробітник лабораторії несе відповідальність за координацію з двома іншими членами групи збору і за реєстрацію зразків, які зібрані (Таблиця 1). ПослеN початковий збір зразків, заповнена форма згоди, кров і трансбуккально тампони передаються співробітнику лабораторії, і записуються ініціали донора, дата народження і інша відповідна інформація, така як тип зразка. Це дозволяє реєструвати числа і типи зразків, зібраних з кожним пацієнтом в процесі збору. Блок-схеми, що підсумовують обробку обох тканин SCC (рисунок 6) і ANT (малюнок 7), є корисними інструментами для навчання нових співробітників процедурам збору.
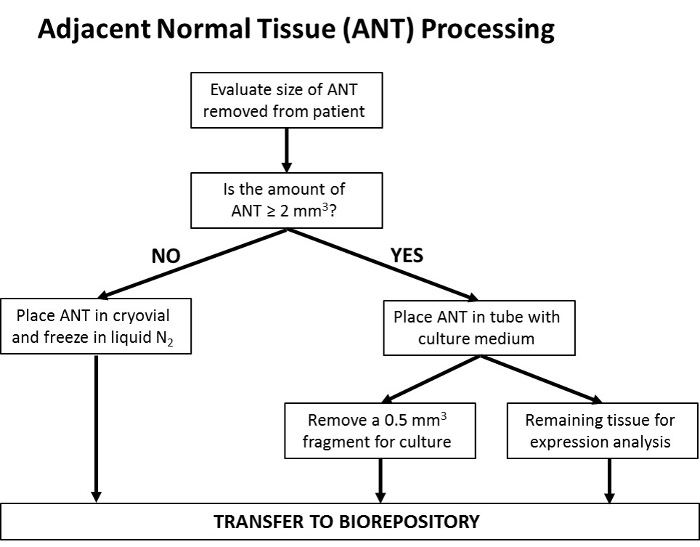
Малюнок 6: Блок-схема, яка визначає обробку зразків SCC. Після видалення пухлини оцінюють розмір зразка. Якщо зразок ≤ 2 мм 3, весь зразок використовується для переробки Мооса, так як оцінка чистих полів (показательУдаленіе повної пухлини) є вищим пріоритетом. Після переробки Mohs будь-яка залишилася тканину заморожується в рідкому азоті і переноситься в біоресурсор. Якщо зразок досить великий, так що частина тканини <> 2 мм 3 може бути видалена, цю частину збирають і поміщають в пробірку, що містить середовище для культивування клітин, а решту використовують для обробки Мооса і зберігають, як зазначено вище. Частина зразка, віддалену в клітинну культуральне середовище, далі сегментируют з видаленням фрагмента ~ 0,5 мм 3 і використовують для встановлення лінії культури клітин; Що залишився фрагмент тканини переноситься в біоресурсор для подальшого аналізу білка і експресії генів. Натисніть тут, щоб переглянути збільшену версію цього малюнка.
er.within-сторінка = "1"> 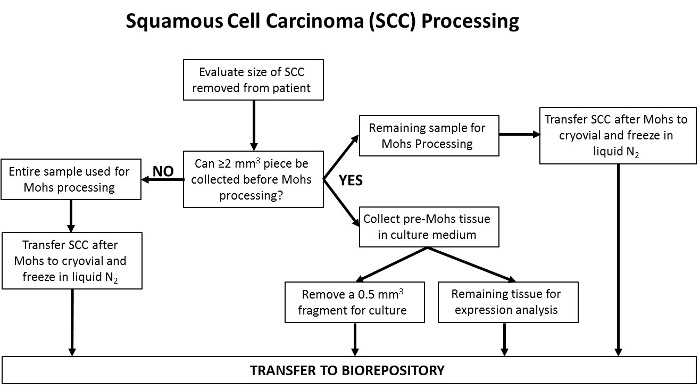
Малюнок 7: Блок-схема, яка визначає обробку зразків ANT. Під час закриття Мооса частина суміжній нормальної тканини (ANT) віддаляється і збирається хірургом Мооса. Якщо розмір зразка становить ≤ 2 мм 3, весь зразок поміщають в криогенну трубку і заморожують в рідкому азоті перед перенесенням в біоресурсор. Якщо зразок> 2 мм 3, весь зразок спочатку поміщають в пробірку, що містить середовище для культивування клітин. Потім зразок додатково поділяють на фрагмент розміром ~ 0,5 мм 3, який використовується для встановлення ліній клітинної культури. Що залишився ділянку тканини переноситься в біоресурсор для зберігання для подальшого аналізу білка і експресії генов.55583 / 55583fig7large.jpg "target =" _ blank "> Натисніть тут, щоб переглянути збільшену версію цього малюнка.
Цей протокол розроблений, щоб мінімізувати відмінності між вибірками в біорекордере. Координація та ефективна комунікація між персоналом клініки і між клініками і всім лабораторним персоналом важливі для мінімізації мінливості і максимального досягнення високоякісних ДНК, РНК і білка з тканин. Незважаючи на те, що ДНК і білок в тканинах є надійними, якщо потрібно РНК, важливо зберігати холодні тканини і в відповідному середовищі під час збору, транспортування та обробки, щоб зберегти цілісність РНК. Точне ведення записів також має життєво важливе значення для зв'язування зразків пацієнтів з їх історією і діагнозом, оскільки ця інформація часто необхідна при аналізі результатів з нижчестоящих додатків.
З ростом інтересу до персоналізованої медицини та біоМаркерних досліджень, нещодавно було створено ряд біорепозіторій. Вони зазвичай пов'язані з лікарняними клініками в великих академічних центрах і вимагають значних витрат на установку та експлуатацію 2,8,19. Створення на базі клініки біоресурси для зразків шкірного раку, створених в рамках повсякденної практики, має кілька ключових переваг в порівнянні з іншими біорепозіторіямі. По-перше, з одного колекцією і вузлом обробки зразків відмінності в обробці зразків, які можуть порушити роботу нижчестоящих додатків, зводяться до мінімуму. По-друге, оскільки ці пожертвування зразки взяті з стабільної популяції пацієнтів, доступ до де-ідентифікованим медичними картками і даними про результати лікування пацієнтів не має аналогів. Ці дані можуть бути анонімізувати і перенесені зі схеми пацієнтів в базу даних біоресурсів під час збору зразків або під час наступного відвідування. По-третє, з лояльною базою пацієнтів, Inic-based biorepository може збирати кілька вибірок від одного і того ж пацієнта, набір зразків, не часто отримується в інших налаштуваннях. Одним з обмежень цього протоколу є те, що він був оптимізований для шкірних проб, отриманих за допомогою мікрографічних хірургії Мооса, і, можливо, його необхідно модифікувати для інших типів тканин або клінічних процедур.
В цілому, однією з ключових цілей біоресурси є надання широкого спектру проб від одного і того ж донора, щоб дослідники могли задавати широкий спектр питань, зокрема, для розробки рідких біопсій і маркерів раку. Зокрема, здатність зіставляти гістологію пухлини і експресію біомаркерів на рівні мРНК та білка із зразками плазми, а також здатність посилатися на дані про результати лікування пацієнта, створює унікальний набір даних. Ми сподіваємося, що модель біоресурсів на базі клінік може бути використана для полегшення нестачі зразків пацієнтів в біомедичних дослідженнях.


