- Йога начинающим видео
- Хулахуп танец видео
- Смотреть моя тренировка видео
- Видео тренировки александра емельяненко
- Как правильно крутить обруч на бедрах видео
- Тренировки в кудо видео
- Тренировки рой джонса видео
- Йога онлайн смотреть видео
- Тренировки костя дзю видео
- Видео тренировки роя джонса
- Видео спинальной
- Айенгар йога видео
- Йога для женщин на видео
- Правильно крутить обруч видео
- Плиометрические отжимания видео
- Новости

Управление Здравоохранения Евпаторийского городского совета (С)2011
67 гостей
Генетичний аналіз ембріонів, ПГД ембріона
- Історія преимплантационной генетичної діагностики (ПГД)
- Як передаються у спадок генетичні захворювання
- Домінантні захворювання:
- Рецесивні захворювання:
- X-зчеплені захворювання:
- Можливі переваги генетичного аналізу
- Кандидати для біопсії ембріона і ПГД
- Пари з повторними невдачами ЕКЗ.
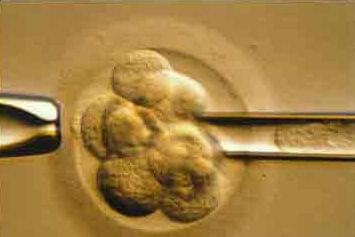
Кожна з 100 трильйонів клітин в організмі людини (за винятком червоних кров'яних клітин) містить весь людський геном. Хромосоми - це струноподобние елементи всередині ядра (в центрі) кожної клітини вашого тіла. Вони містять генетичну інформацію, ДНК. Ген займає певне місце на хромосомі. У нормі, є 23 ідентичних пари хромосом (2 метра ДНК) в кожній клітині, в цілому 46 хромосом. Кожен партнер під час запліднення зазвичай надає 23 хромосоми. Якщо яйцеклітина або сперматозоїд мають аномальну упаковку хромосом, ембріон, який вони створюють, також буде мати хромосомні аномалії. Іноді це пов'язано з перебудовою хромосом, або недоліком частини хромосоми. У деяких випадках є відсутні хромосоми, або додаткова хромосома (анеуплоїдії), що ведуть до спадкових захворювань. Будь ембріон, в якому відсутня хромосома (моносомія) перестане рости до імплантації (фатальна аномалія). Якщо анеуплоїдії включають хромосоми 13, 18, 21, Х або Y, вагітність може дійти до пологів. Найбільш поширеною з цих несмертельних аномалій є трисомія 21, або синдром Дауна, при якій присутня додаткова 21-а хромосома. Інші включають синдром Тернера у жінок і синдром Клайнфельтера у чоловіків.
Історія преимплантационной генетичної діагностики (ПГД)
Перші живорождения після ПГД були зареєстровані в Лондоні в 1989 році. Дві двійні дівчаток-близнят народилися від п'яти пар з ризиком передачі пов'язаного з Х-хромосомою захворювання. В даний час за допомогою методів генетичного аналізу або ПГД можуть бути виявлені близько 90% аномальних ембріонів. Не всі хромосомні або генетичні захворювання можуть бути визначені цими процедурами, так як в ході однієї процедури може бути діагностовано тільки обмежене число хромосом. Численні дослідження на тваринах і деякі дослідження на людині показують, що мікрохірургія ембріона (біопсія), необхідна для видалення клітин, не впливає на нормальний розвиток дитини. Ця процедура, однак, була виконана відносно невеликій кількості пацієнтів у всьому світі, тому точні негативні наслідки, якщо такі є, невідомі. Незважаючи на те, що після генетичного аналізу для виявлення анеуплоїдії всьому світі на сьогоднішній день було народжене вже багато дітей, ця процедура все ще відносно нова. У дослідженнях на тваринах не було виявлено ніяких очевидних проблем і попередні дані з ембріонами людини дозволяють припустити справедливість цього висновку. У дослідженні, проведеному в Університетському коледжі Лондона, дослідники недавно розглянули 12 Попередімплантаційна ембріонів з новою технікою, яка поєднує в собі амплификацию всього генома (WGA) та порівняльну гібридизацію генома (CGH). В результаті в 8 з 12 вивчених ембріонів були виявлені значні хромосомні аномалії. Це може пояснити, чому люди мають в кращому випадку 25% шансів на досягнення життєздатної вагітності в місяць при природному зачатті.
Як передаються у спадок генетичні захворювання
У діаграмах нижче, D або d являє дефектний ген, а N або n представляє нормальний ген. Мутації не завжди призводять до хвороби.
Домінантні захворювання:
Один з батьків має один дефектний ген, який домінує над своїм нормальним парою. Так як нащадки успадковують половину свого генетичного матеріалу від кожного з батьків, є 50% ризик успадкування дефектного гена, і, отже, захворювання.
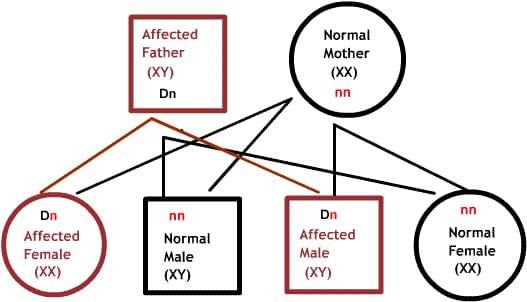
Рецесивні захворювання:
Обоє батьків є носіями одного дефектного гена, але при цьому мають нормальну пару гена. Для успадкування захворювання необхідні дві дефектних копії гена. Кожен нащадок має 50% шанс бути носієм, і 25% шанс успадкувати захворювання.
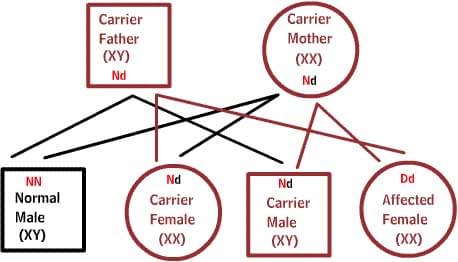
X-зчеплені захворювання:
Нормальні жінки мають XX хромосоми, а нормальні чоловіки XY. Жінки, які мають нормальний ген на одній з Х-хромосом, захищені від дефектного гена на їх інший Х-хромосомі. Однак, у чоловіка відсутня такий захист у зв'язку з наявністю тільки однієї Х-хромосоми. Кожен чоловічої нащадок від матері, яка несе в собі дефект, має 50% шанс успадкувати дефектний ген і захворювання. Кожен жіночий нащадок має 50% шанс бути носієм, як і її мати. (На малюнку нижче X являє нормальний ген а X являє дефектний ген)
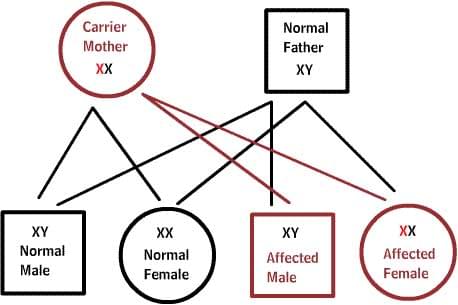
Можливі переваги генетичного аналізу
Попередімплантаційна генетична діагностика дозволяє відібрати і перенести не зміна (хромосомно нормальні) ембріони, які можуть привести до більшої частоті імплантації на ембріон, скорочення втрат вагітності та народження більшої кількості здорових дітей. Генетична діагностика пропонує парам альтернативу болісного вибору з приводу того, щоб перервати постраждалу вагітність після пренатальної діагностики, виробленої шляхом амніоцентезу або біопсії ворсин хоріона (CVS) на більш пізніх стадіях вагітності. Майже всі генетично пов'язані захворювання, які можуть бути діагностовані в перинатальному періоді або амніоцентезом або CVS, можуть бути виявлені і ПГД. Процедура повинна зменшити психологічну травму для пар, які несуть підвищений ризик генетичних захворювань для потомства.
Переваги преимплантационной генетичної діагностики (ПГД) можуть включати в себе:
- Була висунута гіпотеза, що негативний відбір анеуплоїдних ембріонів дозволить поліпшити частоту імплантації, через кореляції між старшим віком матері і хромосомно аномальними ембріонами. Хромосомно нормальні ембріони мають в перспективі більш високі шанси на розвиток. При перенесенні тільки хромосомно нормальних ембріонів в матку, ваші шанси на невиношування можуть зменшитися, а ваші шанси завагітніти можуть збільшитися. Двадцять один відсоток спонтанних абортів обумовлені чисельними хромосомними порушеннями, і основним фактором ризику є вік матері. Трисомії збільшуються з 2% у жінок 25 років до 19% у жінок старше 40 років. За даними ASRM-SART, 52% циклів ЕКЗ в США здійснюється для жінок 35 років і старше, що показує, що популяція ЕКО може отримати велику користь від скринінгу хромосомних анеуплоїдій. Важливо відзначити, що ймовірність настання вагітності і пологів здоровою дитиною, проте, знижується у пацієнтів старше 34 років (як правило, менше 50%) через проблеми, пов'язаних з процедурою ЕКО.
- ПГД в змозі ідентифікувати більшість хромосомних аномалій з ризиком розвитку до пологів. В даний час застосовується ПГД хромосомних аномалії для X, Y, 13, 14, 15, 16, 18, 21 і 22 хромосом. Це становить 70% анеуплоїдій, які виявляються при спонтанних абортах.
- Цілком можливо, що деяка інформація про ваших власних яйцеклітинах і ембріонах може бути корисною для вас в разі подальших спроб ЕКО, або допоможе пояснити минулі невдачі при природному зачатті або ЕКЗ.
- Майбутні пацієнти можуть отримати вигоду з інформації, отриманої від ПГД про зв'язок між хромосомами, що не розвивається або неімплантірующіміся ембріонами.
Можливі ризики генетичного аналізу
- У кращому випадку, за допомогою методів ПГД можуть бути виявлені близько 90% від аномальних ембріонів.
- Щодо велика кількість яйцеклітин або ембріонів можуть бути визнані ненормальними і тому для перенесення залишиться тільки кілька ембріонів. У деяких випадках (11%), може не бути нормальних яйцеклітин або ембріонів. У цих випадках перенесення ембріона не рекомендується. Хоча це і розчаровує результат, цілком ймовірно, що цикл ЕКЗ без ПГД не привів би до вагітності або привів би до аномалій у плода.
- Клітини, які будуть видалені, вивчаються за допомогою спеціалізованих нових методів. Такі процедури іноді не можуть бути проведені через технічні складнощі.
- Не всі хромосомні або генетичні відхилення можуть бути визначені бенкет допомогою даних методів, так як в ході однієї процедури може бути діагностовано тільки обмежене число хромосом.
- Цілком можливо, що нормальний ембріон може бути неправильно визначено як ненормальний, і не перенесений, або що аномальний ембріон неправильно визначено як нормальний і буде перенесений в матку. (ПГД в даний час не є заміною для пренатальної діагностики. Рекомендується проведення пренатальної діагностики для подтверденія діагнозу).
- При видаленні клітин може випадково статися пошкодження ембріона (0,1%).
- Неявні технічні обставини в лабораторії можуть привести до невдачі процесу тестування, що призводить до відсутності результатів. Невдача процесу тестування не робить ніякого впливу на ваш ембріон. В цьому випадку, ембріони для перенесення будуть відібрані на основі існуючих критеріїв.
- Аналіз однієї клітини має свої обмеження. Іноді, хромосомні аномалії знаходяться в одній клітці, але не в інших клітинах того ж ембріона, або навпаки, що виражається мозаїцизмом. Це може призвести до перенесення аномального ембріона, або до відмови від нормального ембріона.
- ПГД для визначення транслокаций може визначити наявність або відсутність певних хромосомних порушень, але не може ні визначити генетичне захворювання, ні передбачити генетичні каліцтва.
- Навіть після успішної процедури ПГД вагітність може не наступити.
Кандидати для біопсії ембріона і ПГД
Кандидати для біопсії ембріона і ПГД включають в себе:
- Жінки старше 34 років: жінки народжуються з усіма яйцеклітинами, які вони будуть коли-небудь мати, і в міру старіння жінки її яйцеклітини піддаються також впливу цього процесу старіння. Таким чином, вірогідність зачаття хромосомно аномального потомство з віком збільшується. В цілому ризик анеуплоїдії збільшується з 1 на 385 у віці 30 років, до 1 на 179 у віці 35 років, до 1 на 63 в віці 40 років, і у віці до 45 років можливість народження хворої дитини становить 1 до 19. В результаті використання ПГД при ЕКЗ стало відомо, що в дійсності больее ніж 20% ембріонів у жінок у віці від 35 до 39 анеуплоїдних, і страждають майже 40% ембріонів у жінок старше 40 років. Більшість з цих ембріонів в разі перенесення в матку або не імплантуються або призводять до невиношування. Це вважається основною причиною низької частоти настання вагітності і пологів жінок у віці 40 років і старше. До впровадження ПГД, для збільшення шансів на зачаття в матку переносилося більше число ембріонів. Як і раніше настійно рекомендується проведення пренатальної діагностики після циклу ЕКЗ, оскільки це підтверджує прогноз нормального потомства. Можливо також, що аномальні ембріони можуть бути помилково визначені як нормальні і перенесені в матку.
- Жінки з рецидивуючою втратою вагітності (звичним невиношуванням): чоловік або жінка пари може мати ненормальну упаковку хромосом, що може викликати фатальні аномалії в деяких вагітностях, але не в інших.
- Пари з транслокаціями: транслокации - це зміни в конфігурації хромосом, при яких хромосоми прикріплюються один до одного (робертсонівські) або ділянки різних хромосомах міняються місцями (взаємні або реципрокні). Приблизно 1 з 900 чоловік має робертсонівські транслокации за участю хромосом 13, 14, 15, 21, 22. Приблизно 1 з 625 чоловік має взаємні транслокації. Для виявлення наявності транслокаций може бути проведено каріотипування обох партнерів. Пари з транслокаціями можуть мати періодичні втрати вагітності, або потомство з психічними чи фізичними проблемами. При збалансованої транслокації, коли немає додаткового або відсутності хромосомного матеріалу, і розрив в хромосомі чи не порушує функції генів, людина не страждає. Носії збалансованих транслокацій можуть бути порушені складними вродженими вадами розвитку, які можуть або не можуть бути пов'язані з спадковим захворюванням. При незбалансованої транслокації, при якій існує або відсутній додатковий матеріал хромосом, окремі особистості, як правило, не будуть порушені, хоча у деяких спостерігатиметься зниження фертильності. Однак існує ризик того, що яйцеклітини або сперматозоїди від такої людини можуть мати незбалансовані транслокації, в результаті чого ембріон буде незбалансованим. Це може привести до невдачі імплантації, повторного невиношування, або потомству з психічними чи фізичними проблемами.
- Пари з аутосомно-домінантними захворюваннями, при яких будуть порушені 50% ембріонів. Пари, які мають дані порушення в сімейному анамнезі, або є носіями, або страждають від успадкованих захворювань.
Пари з повторними невдачами ЕКЗ.
- Пари з історією безпліддя можуть бути в змозі визначити етіологію, і, отже, вибрати відповідне лікування.
- Парам з групи ризику для наслідування потомством хвороби з загрозою для життя, хвороби з пізнім початком (хвороба Хантінгтона), переважно планувати, вибрати відповідні методи лікування, або прискорити процес діагностики (наприклад, ранньої діагностики раку молочної залози)
- Пари, які бажають потомство для виробництва HLA-співпадаючих стовбурових клітин, для страждає дитини зі смертельним захворюванням.
використовувані методи
Для аналізу на наявність генетичних дефектів ембріона, з нього необхідно видалити або перше полярне тільце з незаплідненої яйцеклітини і / або 1 або 2 клітини від кожного ембріона. Це називається біопсією яйцеклітини або ембріона і зазвичай робиться перед тим, як відбувається запліднення, або через 3 дні після запліднення. Біопсія на 6-10 клітинної стадії не робить негативного впливу на Попередімплантаційна розвиток. На цьому етапі кожна клітина має повний набір хромосом. Зазвичай з ембріона видаляється лише одна клітина, так як очікується, що будуть однаковими з усіма іншими клітинами в ембріоні. Іноді необхідно видалити другу клітку з ембріона, наприклад, якщо сигнал в першою не виявлено. Для діагнозу схильності за допомогою першого і другого полярних тілець, як показників генетичного статусу яйцеклітини, використовується аналіз методом FISH. Недоліком аналізу полярних тілець полягає в тому, що він не бере до уваги батьківські анеуплоїдії.
Аналіз біопсірованной клітини використовує один з двох методів:
- Флуоресцентна гібридизація in situ (FISH): біопсірованной клітина фіксується на предметному склі, нагрівається і охолоджується, і її ДНК "позначається" кольоровими флуоресцентними барвниками, званими зондами (маленькі шматочки ДНК, які відповідають досліджуваним хромосомами), по одному для кожної обумовленою хромосоми. В даний час може бути ідентифіковано 8 з 23 хромосом. Після завершення ембріолог враховує кольору під потужним мікроскопом і в стані, в більшості випадків, відрізнити нормальні від аномальних клітин. Цей процес займає близько доби. Нормальні ембріони будуть або перенесені в матку на 4-й день після пошуку яйцеклітин, або піддадуться продовженим культивування і будуть перенесені на 5-й день, як бластоцисти. Клітини, що використовувалися для ПГД, більше не життєздатні, і не будуть повернуті в ембріон, але можуть бути збережені для майбутніх досліджень.
- Полімеразна ланцюгова реакція (ПЛР): методика, яка збільшує кількість копій специфічних регіонів ДНК, щоб виробити достатню для аналізу кількість ДНК. ДНК є двухцепочечной (за винятком деяких вірусів), і два ланцюги з'єднуються дуже специфічним чином. "Послідовність цеглинок" генів являє собою певний порядок появи 4-х різних дезоксирибонуклеотидов в сегменті ДНК. Ці 4 компонента: аденін (А), тимидин (T), цитозин (C), і гуанін (G). Послідовність цього 4-літерного алфавіту генерує складу гена. При цій методиці ДНК нагрівають (денатурують), щоб розділити 2 нитки. Далі додаються праймери і ДНК охолоджується, з тим щоб знову утворилися подвійні нитки. Потім в цикли додають ферменти, які можуть "прочитати" послідовність гена, що призводить до множення ДНК. ПЛР використовується для діагностики ген-специфічних захворювань, так само як і для виявлення хвороботворних вірусів і / або бактерій, або в криміналістиці в зв'язку з підозрою в скоєнні злочину.


