- Йога начинающим видео
- Хулахуп танец видео
- Смотреть моя тренировка видео
- Видео тренировки александра емельяненко
- Как правильно крутить обруч на бедрах видео
- Тренировки в кудо видео
- Тренировки рой джонса видео
- Йога онлайн смотреть видео
- Тренировки костя дзю видео
- Видео тренировки роя джонса
- Видео спинальной
- Айенгар йога видео
- Йога для женщин на видео
- Правильно крутить обруч видео
- Плиометрические отжимания видео
- Новости

Управление Здравоохранения Евпаторийского городского совета (С)2011
67 гостей
Тестування акваріумний води

У прісноводому акваріумі з особливо чутливими рослинами і рибою значення pH і концентрація нітратів повинні перевірятися регулярно (приблизно раз в 15 днів). Жорсткість води можна перевіряти з великими інтервалами, але якщо помічений сильний рівень випарів, перевірку варто проводити частіше. При уповільненні зростання рослин або при введенні добрив необхідно перевірити залізо. 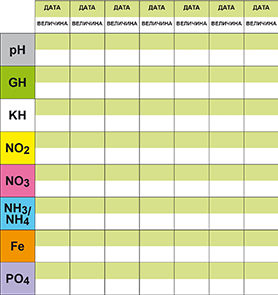
Якщо Ви є власником акваріума з солоною водою, то необхідна регулярна перевірка рівня pH (приблизно раз в тиждень) і нітратів (приблизно кожні 15 днів). Залежно від чутливості мешканців (особливо безхребетних) також необхідністю може стати регулярна перевірка карбонатної жорсткості - мінімум кожні 15 днів. Інші показники, такі як залізо, фосфати, нітрати і амоній / аміак, необхідно перевіряти в разі, якщо виникають проблеми в поведінці мешканців (нерегулярне розкриття восьминога, дивна поведінка риб і т.д.).
У будь-якому випадку важливо вести щоденник і записувати спостережувані показники. Таким чином, буде отриманий певний досвід і час проведення перевірок буде більш очевидно.  Рівень pH в прісній воді
Рівень pH в прісній воді
Рівень pH є водневим показником кислотності середовища, який відображає кількість водню і гідроксильних іонів, присутніх в воді. Вода з показником від 0 до 7 умовно вважається кислою, 7 - нейтральної, від 7 до 14 - лужний. Це теоретична схема, але з практичної точки зору акваріумісти-любителі повинні пам'ятати, що всі водні організми, як риби, так і рослини або мікроорганізми, адаптовані до життя у воді з точними показниками pH. Залежно від чутливості окремих організмів, навіть невелике відхилення від «ідеального» показника може негативно вплинути на їх існування.
 Важливо! Між двома різними показниками pH існує велика різниця; водне число з рівнем pH рівним 5 в 10 разів більше кислотно, ніж водне число з показником pH 6.
Важливо! Між двома різними показниками pH існує велика різниця; водне число з рівнем pH рівним 5 в 10 разів більше кислотно, ніж водне число з показником pH 6.
Для прісноводних акваріумів важливо наступне:
• Показник від 6.8 до 7.2 підходить для розведення більшості риб і акваріумних рослин.
• Деякі види риб (пецилієві, цихловие) потребують рівні pH більше 7.
• Рівень pH менше 5.5 небезпечний для всіх видів риб (навіть для тих, які мешкають в кислотних водах).
• При рівні pH 7.5 і вище більшість рослин страждають від нестачі CO2, в зв'язку з чим можуть припинити своє зростання.
Більш детально ... Відповіді на найчастіші запитання - рН 
 Загальна жорсткість - GH
Загальна жорсткість - GH 
Загальна жорсткість являє собою сумарну концентрацію іонів кальцію (Ca) і магнію (Mg). Вона утворюється з двох складових - карбонатної (тимчасової) і некарбонатних (постійної) жорсткості. Карбонатная, інша назва - сульфатна жорсткість, обумовлена наявністю у воді гідрокарбонатів (і карбонатів при рН 8.3) кальцію і магнію. При кип'ятінні води гідрокарбонати розкладаються, утворюючи погано розчинний карбонат кальцію, вуглекислий газ і воду. Тимчасову твердість можна зменшити або повністю усунути шляхом тривалого кип'ятіння. Жорсткість ж, що зберігається в воді після кип'ятіння, називається постійної некарбонатних жорсткістю. Її утворюють сульфати, хлориди, нітрати, силікати і фосфати, і її значення не можна зменшити, просто прокип'ятивши воду.
В акваріумістики для найбільш точних вимірювань жорсткості води важливо вимірювати загальну жорсткість (GH), а також карбонатні жорсткість (KH) і враховувати обидві ці незалежні величини. Загальна жорсткість прісної води повинна бути в 3 - 4 рази вище, ніж карбонатна жорсткість, досягаючи величин від 5 до 10 ° GH. Для риб, що мешкають в природі в жорсткій воді, величина повинна бути більше 12 ° GH.  Карбонатна жорсткість - KH
Карбонатна жорсткість - KH
Карбонатна жорсткість (виражається в ° KH) показує наявність карбонатів, а також кальцію і бікарбонатів магнію, і становить частину так званої загальної жорсткості (яка виражається в ° GH). Більш сучасне і правильне позначення, яке проте не таке поширене в світі акваріумістики, трактує замість карбонатної жорсткості цю величину як «буферну ємність кислотності до 4.3» в ммоль / л, де 1 ° KH дорівнює 0.36 ммоль / л.
Карбонатна жорсткість відіграє особливу роль в хімічному рівновазі води через свій тісний зв'язок з величинами pH і вуглекислого газу. З цієї причини її перевірка важлива як в прісній воді для культивації рослин і розведення чутливих видів риб, що мешкають в м'якій воді, так і в морській воді для стійкого рівня pH більше 8, а також для харчування безхребетних.

У прісній воді карбонатні жорсткість повинна по можливості досягати 4 ° KH (більш низькі величини роблять рівень pH нестабільним, в той час як більш висока величина може створювати проблеми для культивації рослин). У морській воді карбонатні жорсткість повинна знаходитися в діапазоні від 8 ° KH до 10 ° KH.
Для того, щоб знизити карбонатні жорсткість в прісній воді (часто є необхідним заходом, оскільки питна вода завжди жорсткіше) можна пропустити її через фільтр з глини або через засіб зі спеціальних синтетичних смол (можливе використання прямо в фільтрі), найпростіший спосіб - використовувати установку зворотного осмосу.
Зазвичай протилежна проблема виникає в морській воді: після певного періоду часу карбонати, які були спожиті, необхідно буде інтегрувати повторно за допомогою додавання спеціальних хімічних продуктів. 
 Амоній - NH4
Амоній - NH4
Будь-акваріум неодмінно містить органічні відходи через екскрементів риб, метаболізму мікроорганізмів і залишків їжі, а також частинок рослин і водоростей. Всі ці речовини забруднюють воду, але вони також корисні для життєдіяльності деяких типів бактерій та інших мікроорганізмів, які є невід'ємною частиною біологічного циклу, званого "азотним циклом".
Для того, щоб гарантувати ідеальне середовище існування для всіх організмів, що живуть в акваріумі, цей цикл повинен здійснюватися без вироблення токсичних речовин, тобто без розпаду органічних продуктів. Першим кроком є трансформація білкових речовин в амоній / аміак за допомогою спеціальних бактерій. Залежно від рівня pH в даному процесі, амоній виробляється (NH4), коли рівень pH приблизно дорівнює 7 або менше, в той час як при рівні pH вище 7.5 крім амонію також виробляється аміак.
Аміак досить токсичний, а амоній менш небезпечний, і більш того він частково усувається за допомогою рослин і нижчих водоростей, які використовують його як джерело азоту. Концентрація амонію в прісній воді 0.10 - 0.50 мг / л є нормальною і безпечною. У випадку з аміаком кількість більш 0.02 мг / л є небезпечним, а при 0.20 мг / л мають місце випадки загибелі риби і безхребетних. Високий рівень амонію / аміаку викликаний недостатньою системою фільтрації (пошкодженої або недостатньо зрілої бактеріальної флорою), перенаселенням в резервуарі, надмірною кількістю корму.
Для надто високій концентрації амонію / аміаку особливо важливо усунення причини (за допомогою запуску системи фільтрації, перевірки щільності популяції, обмеження запасів корму). У непередбачених ситуаціях важливо частково змінити воду.  Нітрити - NO2
Нітрити - NO2 
Нітрити є другим «маленьким кроком» на шляху азотного циклу і утворюються при переробці амонію / аміаку бактерією Nitrobacter. У прісній воді їх концентрація є нормальною від 0.02 до 0.10 мг / л, концентрація 0.20 мг / л (якщо вона не взята з уже «забрудненої» питної води) є показником того, що система фільтрації працює не ідеально; показник більш 0.50 мг / л є явним сигналом небезпеки.
Іноді певні види риб все ж переносять концентрацію навіть в 0.20 мг / л. У морській воді, особливо при великій кількості безхребетних, концентрація в 0.05 мг / л не повинна бути перевищена, а 0.10 мг / л є летальними для певних чутливих морських організмів.  Нітрати - NO3
Нітрати - NO3
На третьому етапі переробки (мінералізації) органічних речовин у воді в акваріумі виробляються нітрати. Нітрати мають обмежену токсичність для риби, але їх наявність значно полегшує поширення нижчих водоростей. Певна концентрація нітратів завжди присутній (питна вода, наприклад, може містити до 50 мг / л відповідно до європейських законів). Рекомендується не перевищувати 80 мг / л в прісній воді, але деякі чутливі риби повинні жити в воді з концентрацією нижче 20 мг / л.

Навіть морська риба досить толерантна, особливо якщо вона повільно адаптується до зростаючої концентрації, але важливо не перевищити концентрацію в 50 мг / л. Морські безхребетні, особливо певні типи коралів, мають різні вимоги, максимальна концентрація досягається при 20 мг / л. Нітрати можуть бути усунені при використанні спеціальних фільтрів або часткової заміни води.
Часто високий вихідний показник у питній воді може привести до необхідності негайної обробки цієї води (установці зворотного осмосу, фільтрації за допомогою синтетичних смол).  Фосфати - PO4
Фосфати - PO4
 Фосфати є сполуки фосфору (солі фосфорних кислот). Також як і залізо, фосфати життєво важливі для всіх акваріумних тварин і рослин. Рибки використовують фосфор при побудові свого організму (нервової, кісткової та інших систем), а для вищих рослин фосфор взагалі є найважливішим макроелементом, правильний розвиток без якого просто неможливо. Навіть велика концентрація фосфатів не смертельна для акваріумних риб, але його надлишок неминуче призведе до активного росту найпростіших водоростей, що не зможе не позначитися на вищих рослинах. Зазвичай акваріумна вода містить занадто високу концентрацію фосфатів, які потрапляють туди з залишками корму і з екскрементів риб, тому особливо важливо проводити регулярне тестування.
Фосфати є сполуки фосфору (солі фосфорних кислот). Також як і залізо, фосфати життєво важливі для всіх акваріумних тварин і рослин. Рибки використовують фосфор при побудові свого організму (нервової, кісткової та інших систем), а для вищих рослин фосфор взагалі є найважливішим макроелементом, правильний розвиток без якого просто неможливо. Навіть велика концентрація фосфатів не смертельна для акваріумних риб, але його надлишок неминуче призведе до активного росту найпростіших водоростей, що не зможе не позначитися на вищих рослинах. Зазвичай акваріумна вода містить занадто високу концентрацію фосфатів, які потрапляють туди з залишками корму і з екскрементів риб, тому особливо важливо проводити регулярне тестування.
У прісній воді важливо, щоб рівень фосфатів не опускався нижче 0.02 мг / л, так як рослинам для правильного росту і побудови своїх клітин просто необхідний фосфат.
Варто відзначити, що найчастіше питна вода містить високу кількість фосфатів (навіть більше 5 мг / л). У цьому випадку важливо заздалегідь правильно обробити воду до її потрапляння в акваріум, використовуючи зворотний осмос або спеціальні смоли. 
 Залізо - Fe
Залізо - Fe
Залізо є обов'язковим елементом для будь-яких тварин і рослин. У природних водоймах концентрація заліза значно відрізняється в залежності від різних біотопів, але тим не менше завжди присутній.
Залізо у воді є в двох різних формах, в залежності від електричного заряду іонів - двовалентне залізо (Fe2 +) і тривалентне залізо (Fe3 +). Двовалентне залізо може бути розчинено у воді, в той час як тривалентне залізо зазвичай не розчиняється. Тільки залізо, розчинена у воді, може абсорбуватися рослинами, морськими водоростями або мікроорганізмами. На жаль, коли кисень (необхідний для акваріума) присутній в залозі, воно перетворюється в тривалентне залізо і приєднується до інших речовин, при цьому стає марним. Часто воно сприяє формуванню блідо-жовтого нальоту на фільтрі. Для того, щоб перешкодити цій неприємності, залізо необхідно помістити в акваріум в спеціальній формі, тобто спільно з хелаторамі, які формують щільні хімічні сполуки, роблячи залізо розчиняється навіть у воді і тим самим доступним для різних водних організмів.
 Зазвичай рідинні індикатори для вимірювання заліза вимірюють тільки двовалентне залізо. Для перевірки наявності всього заліза (навіть хелатного заліза) певні вимірювачі містять реагенти, які «ламають» хелат, перетворюючи приховане залізо в «видиме».
Зазвичай рідинні індикатори для вимірювання заліза вимірюють тільки двовалентне залізо. Для перевірки наявності всього заліза (навіть хелатного заліза) певні вимірювачі містять реагенти, які «ламають» хелат, перетворюючи приховане залізо в «видиме».
У прісній воді рівень заліза повинен варьіроватьcx від 0.03 мг / л до 0.10 мг / л для забезпечення здорового росту рослин. Рівень вище 0.2 мг / л небезпечний як для рослин, так і для багатьох риб. Завдяки тестуванню води Ви можете перевірити воду в своєму акваріумі і вжити необхідних заходів.
У морській воді концентрація повинна варіювати від 0.05 мг / л до 0.1 мг / л.
джерело: www.prodacinternational.it
Адаптація тексту: В.Люфт для akvabluz.ru


