- Йога начинающим видео
- Хулахуп танец видео
- Смотреть моя тренировка видео
- Видео тренировки александра емельяненко
- Как правильно крутить обруч на бедрах видео
- Тренировки в кудо видео
- Тренировки рой джонса видео
- Йога онлайн смотреть видео
- Тренировки костя дзю видео
- Видео тренировки роя джонса
- Видео спинальной
- Айенгар йога видео
- Йога для женщин на видео
- Правильно крутить обруч видео
- Плиометрические отжимания видео
- Новости

Управление Здравоохранения Евпаторийского городского совета (С)2011
67 гостей
Клінічні та морфометричні предиктори загоєння трофічних виразок нижніх кінцівок у пацієнтів з цукровим діабетом
- Вступ Швидке зростання поширеності цукрового діабету (ЦД) 2-го типу послужив підставою для експертів...
- Клінічна характеристика груп порівняння
- Клінічна характеристика груп порівняння
- Результати дослідження та їх обговорення
- Висновки
Вступ
Швидке зростання поширеності цукрового діабету (ЦД) 2-го типу послужив підставою для експертів ВООЗ оголосити пандемію цього захворювання. За прогнозом фахівців ВООЗ, до 2025 року кількість хворих на діабет має досягти 380,0 мільйона чоловік [1]. Одним з найбільш частих і важких хронічних ускладнень ЦД є ураження нижніх кінцівок, яке визначається як синдром діабетичної стопи (СДС). Поразки кінцівок у хворих на діабет є основною причиною інвалідності цих пацієнтів і завдають серйозної соціально-економічних збитків. Несвоєчасна діагностика СД і СДС, а також неправильна лікувальна тактика призводять до ускладненого перебігу захворювання та ампутації кінцівок, які фактично в світі виконуються кожні 30 секунд [2].
Аналіз структури уражень нижніх кінцівок за даними різних досліджень переконливо продемонстрував, що трофічні виразки відносяться до найбільш частого прояву СДС і виявляються у 4-10% хворих [3]. Частота ампутацій кінцівок становить від 6 до 8 випадків на рік на 1000 хворих на ЦД [4]. Тяжкість ураження кінцівок при СДС призводить до двократного збільшення смертності цих хворих в порівнянні з пацієнтами без цього ускладнення діабету, а найбільш несприятливий прогноз мають перенесли ампутацію.
Крім серйозного прогнозу щодо життя пацієнта, ампутація є високовитратною частиною витрат охорони здоров'я, так, якщо вартість первинного загоєння виразки становить $ 7-17 тис., То витрати, пов'язані з ампутацією нижньої кінцівки, досягають $ 30-60 тис. У Росії прямі витрати на ампутацію приблизно такі ж істотні і еквівалентні $ 1000-1200 [2]. Важливим для клінічної практики є доведений факт, що 85% ампутацій можуть бути запобігти при ранньому виявленні СДС і проведенні нескладних профілактичних заходів, що знижують ризик утворення виразки, а також при правильному лікуванні вже виникла виразки.
Епідеміологічні дослідження останніх років не викликають сумнівів у необхідності вироблення заходів щодо запобігання і зниження частоти ампутацій у хворих на ЦД, а також з вивчення та впровадження нових способів місцевого лікування виразкових дефектів.
Особливий інтерес викликають препарати, що покращують імунний статус в області трофічної діабетичної виразки. При СД існує дисфункція макрофагів, що супроводжується зниженням вироблення цитокінів і факторів росту, що мають велике значення в процесі репарації. До сучасних імуномодулюючих препаратів відноситься група бета-глюканов, є гомополісахаридів, що складаються з бета-D-глюкопіразоніл одиниць. Розчинна препарат бета-1,3 / 1,6-глюкан, яку виробляє компанія «Біотек Фармакон» (Норвегія), що виробляється з дріжджів Saccharomyces cerevisiae, є найбільш активним полисахаридом, що підсилює функцію макрофагів і прискорює процес загоєння ран. Завдяки здатності розчинної бета-1,3 / 1,6-глюкана активувати і нейтралізувати дефекти макрофагів, наявні при цукровому діабеті, застосування його на область діабетичної виразки повинно забезпечити прискорення її загоєння до повної епітелізації рани.
Також актуальними проблемами в клінічній практиці лікування діабетичних виразок залишаються предиктори загоєння і несприятливого прогнозу, особливо для пацієнтів з високим ризиком ампутації. Все вищевикладене і визначило актуальність проблеми, мета і завдання цього дослідження.
Мета дослідження - виявити особливості клінічного фенотипу пацієнта з цукровим діабетом, що має трофічну виразку нижніх кінцівок і встановити фактори, що впливають на швидкість і вірогідність її повного загоєння, в тому числі визначити безпеку і ефективність місцевого використання розчинної гелю бета-1,3 / 1,6 -глюкана в порівнянні з гелем-плацебо і стандартним алгоритмом лікування.
Матеріали і методи дослідження
Проведення порівняльної оцінки епідеміологічної ситуації в Архангельській області з метою визначення поширеності трофічних виразок нижніх кінцівок при цукровому діабеті, частоти виконання малих і великих ампутацій при ускладненому перебігу синдрому діабетичної стопи проводилося за даними загальноросійського і Архангельського регістрів цукрового діабету, опублікованих в монографії, узагальнюючої досвід 5 річної діяльності науково-практичного проекту «Мобільний діабет-центр». Виконувався аналіз поширеності діабетичної нейропатії і проявів синдрому діабетичної стопи, а також порівняння частоти виконання малих і великих ампутацій в РФ і в Архангельській області. Проводився аналіз ампутацій, виконуваних в профільному відділенні лікування хворих СДС (2-е хірургічне відділення) Першої міської клінічної лікарні швидкої медичної допомоги (ПГКБ СМП) м Архангельська за період з 2006 по 2008 рік. Була проведена оцінка роботи кабінету діабетичної стопи, який функціонує в складі ДЕЦ, з аналізом щорічних звітів відвідуваності і структури виявляється патології у пацієнтів з цукровим діабетом.
Крім того, в дослідження були включені 23 пацієнта з нейроішеміческіе і Нейропатіческой виразками нижніх кінцівок. Стаж захворювання на цукровий діабет в середньому становив 18,70 ± 12,50 року. Первинний відбір пацієнтів здійснювався на підставі критеріїв включення і виключення серед хворих на цукровий діабет з трофічними виразками нижніх кінцівок в кабінеті «Діабетична стопа» Першої міської клінічної лікарні швидкої медичної допомоги м Архангельська (головний лікар - народний лікар СРСР Е.Е. Волосевич) в період з 2003 по 2004 рік. Даний етап роботи був сліпим рандомізованих дослідженням первинної оцінки можливості використання гелю розчинної бета-1,3 / 1,6-глюкана для місцевого лікування у пацієнтів з діабетичними виразками. Бета-1,3 / 1,6-глюкан є найбільш активним полисахаридом, стимулюючим функцію макрофагів, запатентований і проводиться компанією «Біотек Фармакон» (Норвегія). Дія препарату на імунну систему відбувається через рецептори розпізнавання структури фагоцитів, що запускає серію внутрішньоклітинних сигналів, приводячи до активації клітин і утворення ефекторних молекул вродженого імунної відповіді, включаючи хемокіни, цитокіни, антимікробні речовини, і їх перетворення в ефективні кілери мікробних агентів і стимулятори процесу загоєння . Було висловлено припущення, що бета-1,3 / 1,6-глюкан може сприяти більш швидкому загоєнню діабетичних трофічних виразок 1-2-го ступеня тяжкості за класифікацією Вагнера.
Критерії включення: інформовану згоду на участь в дослідженні, вік хворих від 18 до 80 років, наявність цукрового діабету, збереження дистального артеріального кровотоку (лодижечно-плечовий індекс (ЛПІ) не менше 0,7), наявність хронічної виразки нижніх кінцівок, купірування проявів інфекції або целюліту в області кінцівки до рандомізації в дослідження, первинна хірургічна обробка виразки з видаленням некротизованих тканин до рандомізації в дослідження, розміри виразки повинні бути більше 1 см2 і менше 40 см2.
Критерії виключення: наявність остеомієліту в області виразки, сумарна площа всіх виразок, що перевищує 100 см2; наявність супутньої патології, при якій необхідно використовувати такі види терапії, як опромінення, або хіміотерапія, або застосування імунодепресантів і кортикостероїдів; вагітність або годування; жінки фертильного віку, які не застосовують оральну гормональну контрацепцію.
Біохімічні тести проводилися для оцінки якості контролю СД (глікірованний гемоглобін, глікемія натще), ниркової функції (креатинін), дисліпідемії (загальний ХС, ЛПНЩ, ТГ) на апараті COBAS MIRA PLUS і наявності запального синдрому (ШОЕ, лейкоцитоз) на апараті Hemolux AUTO hematology analyzer. Лодижечно-плечовий індекс вимірювали методом допплероманометріі за допомогою індикатора ультразвукової допплерівської швидкості кровотоку «Мінідоп» фірми «Біосс». Нейропатіческой виразки вважалися при наявності у пацієнта дистальної нейропатії і ЛПІ в межах 0,9-1,1. При ЛПІ в межах 0,9-0,7 додатково виконували дуплексне сканування судин нижніх кінцівок ультразвуковим апаратом ALKA 4000 лінійним датчиком 10 мГц для виключення клінічно значущих окклюзий і стенозів судин. Виконувалися стандартні тести для діа-гностики тактильної, температурної, больовий, вібраційної чутливості, рефлексів. Оцінювалися несприятливі події в ході дослідження.
Клінічна характеристика груп порівняння
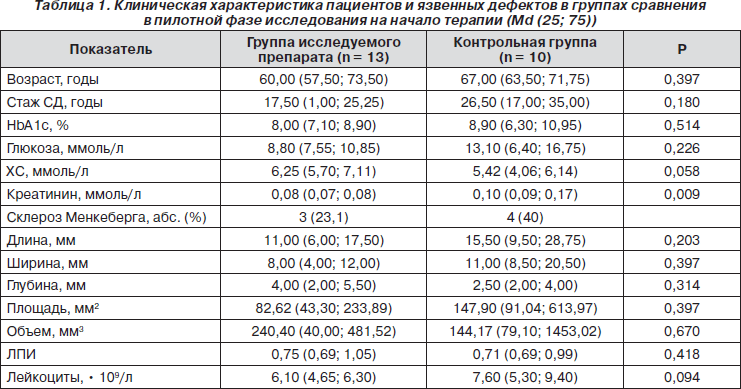
У більшості пацієнтів були такі судинні ураження: ІХС - у 5 хворих, облітеруючий атеросклероз нижніх кінцівок - у 8. Мікросудинних ускладнення були зареєстровані у 21 хворого: у 12 з них відзначалася діабетична нефропатія, у 10 - діабетична ретинопатія. Групи порівняння не мали достовірних відмінностей за віком і тривалості захворювання, біохімічними показниками, клінічним особливостям і розмірами виразки (табл. 1). У всіх пацієнтів був незадовільний контроль цукрового діабету, дисліпідемія, деякі хворі мали діабетичну нефропатію. Стан кровопостачання нижніх кінцівок було порівняти в обох групах: по 2 нейроішеміческіе виразки в кожній групі, 11 нейропатических виразок в групі досліджуваного препарату і 8 - в групі порівняння. За результатами додаткового обстеження не було діагностовано критичних стенозів і оклюзій судин. Таким чином, ми мали можливість правильно оцінити вплив досліджуваного препарату на процес загоєння виразкових дефектів щодо стандартної місцевої терапії виразок, а також виявити клінічно значущі фактори, що впливають на швидкість цього процесу.
Після завершення пілотної фази і підтвердження первинної гіпотези про можливість використання досліджуваного препарату для місцевого лікування діабетичної трофічної виразки нижньої кінцівки було прийнято рішення про виконання подвійного сліпого клінічного дослідження з метою оцінки ефективності та безпеки цього препарату щодо використання плацебо. Друга фаза дослідження виконувалася в період з 2005 по 2007 рік на базі кабінету «Діабетична стопа» при ДЕЦ р Архангельська. Протокол і дизайн другої фази дослідження були складені та затверджені відділом клінічних досліджень компанії Biotec Pharmacon ASA (м Осло, Норвегія), схвалені Національним етичним комітетом РФ і Комітетом з етики ГОУ ВПО СГМУ.
Критерії включення: наявний у пацієнта цукровий діабет 1-го або 2-го типу; вік пацієнта більше 18 років; наявність виразки, розташованої на ступні або в області нижньої третини гомілки, існуючої як мінімум 4 тижні до включення і відповідної 1-й або 2-го ступеня за класифікацією Вагнера; адекватне кровопостачання кінцівки, підтверджене ЛПІ не менше 0,7; розміри досліджуваної виразки> 1,0 см2, але <20,0 см2; підписану інформовану згоду.
Критерії виключення: вагітність, або лактація, або відсутність адекватної контрацепції для фертильних жінок; тяжке недоїдання; клінічні ознаки гангрени кінцівки; активна або велика флегмона; активний остеомієліт ступні з досліджуваної виразкою; некроз пальців на стопі з досліджуваної виразкою; хірургічні процедури (за винятком санації) на ступні з досліджуваної виразкою, що виконуються протягом останніх 21 дня, що передують візиту скринінгу; досліджувана виразка в області суглоба Шарко; ознаки інфікування глибоких тканин в досліджуваній виразці на 0-му візиті; якщо неісследуемая виразка розташовується на досліджуваній стопі, ближче 5 см від досліджуваної виразки на 0-му візиті; рівень глюкози в крові при випадковому вимірюванні> 25,0 ммоль / л, зловживання алкоголем або наркотиками.
Біохімічні тести, допплероманометрія і дуплексне сканування судин нижніх кінцівок були виконані на тій же апаратурі, яка була використана в пілотній фазі дослідження.
Клінічна характеристика груп порівняння
Групи порівняння другої фази не розрізнялися за статтю, віком, антропометричними показниками, стажу захворювання (табл. 2). У 18 пацієнтів були прояви діабетичної ретинопатії. Нефропатія мала місце у 24 хворих: стадія мікроальбумінурії зареєстрована в 12 випадках, протеїнурії - в 7, в 5 випадках була діагностована хронічна ниркова недостатність. У 17 хворих була ІХС, а 3 пацієнта перенесли ГПМК (більше 6 місяців назад). В обох групах переважали нейропатичні виразки: 12 - в групі досліджуваного препарату, 9 - в групі «плацебо»; у 5 пацієнтів відзначені нейроішеміческіе виразки в групі досліджуваного препарату і у 7 - в групі «плацебо»; 9 виразок були розташовані в області гомілки, з них 4 - у пацієнтів групи досліджуваного препарату і 5 - конт- рольної групи, а особливістю цих виразок було поєднання в патогенезі діабетичної нейропатії з варикозної хворобою нижніх кінцівок. Склероз Менкеберга був у 7 пацієнтів в групі досліджуваного препарату і у 8 - в групі плацебо. Групи порівняння не розрізнялися за рівнем лодижечно-плечового індексу, складу мікрофлори виділень трофічної виразки, а також за розмірами і локалізації виразкових дефектів на момент початку терапії. Ні у кого з пацієнтів не було виявлено клінічно значущих стенозів артерій ниж-них кінцівок. У всіх пацієнтів були прояви хронічної декомпенсації цукрового діабету у вигляді гіперглікемії і підвищеного рівня глікозильованого гемоглобіну, були симптоми запалення: помірно підвищений рівень лейкоцитів, збільшена ШОЕ, підвищення СРБ (табл. 2).

Математична обробка даних проводилася за допомогою програми SPSS for Windows v.13. Всі дані були перевірені на нормальність розподілу. Кількісні ознаки, що мають нормальний розподіл, позначалися як середнє зі стандартним відхиленням (M; SD), що не мають нормального розподілу - як медіана Md (25-й, 75-й перцентілі). При порівнянні статистичних гіпотез використовували критичний рівень значимості р <0,05. У роботі застосовували дисперсійний аналіз АNОVА і непараметричний тест Манна - Уїтні для порівняння незалежних груп. Первинні кінцеві точки були отримані за допомогою аналізу виживаності зі змінною «дні» до повного загоєння виразок і виражені за допомогою кривих виживання Каплана - Майера, лог-ранк-тесту. Медіана і середній час до повного загоєння і 95% інтервали були отримані в результаті статистичної обробки даних. Внесок препарату в загоєння трофічної виразки за певний відрізок часу був встановлений за допомогою регресійного аналізу Кокса з отриманням 95% інтервалів. Таким же чином були виявлені клінічні предиктори загоєння діабетичної виразки. Побудовано регресійні моделі впливу клінічних факторів і досліджуваного препарату на процеси загоєння виразок за допомогою регресії Кокса. Вторинні кінцеві точки були визначені по динаміці зменшення розмірів в порівнюваних групах за допомогою тестів Манна - Уїтні і Уилкоксона. Були встановлені відносні фактори ризику появи нових виразкових дефектів і можливих ампутацій через рік від початку спостереження за пацієнтами в обох групах.
Результати дослідження та їх обговорення
У хворих на ЦД 1-го типу частка малих ампутацій в Архангельській області незначно перевищувала дані показники по РФ, але калічать пацієнта високі ампутації зустрічалися частіше (табл. 3).

Як випливає з представлених в табл. 4 даних, в когорті хворих на ЦД 2-го типу в Архангельській області поширеність діабетичної нейропатії і синдрому діабетичної стопи була в 3 рази менше в порівнянні з даними по РФ. Малі ампутації виконувалися в 2 рази менше в нашому регіоні, в той час як великі ампутації нижніх кінцівок зустрічалися в 7 разів більше, ніж за даними в РФ.

За даними регістра Архангельської області (М.А. Старцева, 2009), на протязі останніх 6 років зберігається велика частота високих ампутацій нижніх кінцівок (29-35 нововиявлених випадків на рік).
Аналіз звітів 2-го хірургічного відділення ПГКБ ШМД м Архангельська за останні 3 роки дозволив встановити, що частота ампутацій і кількість ліжко-днів у хворих СДС в цьому відділенні була вище, ніж в Архангельській області (за даними регістра), але при цьому частка високих ампутацій була на 33% менше. Упевнена тенденція зниження загальної кількості високих ампутацій у м Архангельську з'явилася останнім часом і була обумовлена впровадженням міждисциплінарного підходу до лікування та профілактики трофічних виразок в цьому провідному клінічному закладі (табл. 5).

Аналіз річніх звітів підрозділів стаціонару та амбулаторного ланки НЕ дает возможности точно оцініті пошіреність діабетічніх віразок и ампутацій у хворого на ЦД в межах м Архангельський и области. Велика частота високих ампутацій кінцівок в Архангельській області у хворих на ЦД свідчить про відсутність профілактичних заходів в когорті пацієнтів з факторами ризику СДС.
До кінця лікувального періоду в групі досліджуваного препарату повністю зажили 12 виразкових дефектів з 13, а в контрольній групі - 4 з 10. Медіана часу повного загоєння діабетичної виразки була 35 днів в групі досліджуваного препарату (Md = 35,00 (17,50; 80 , 50)) і 84 дня (Md = 84,00 (28,00; 84,00)) в групі порівняння відповідно (р = 0,072). При аналізі часу загоєння виразок за допомогою кривих виживання Каплана - Майера і лог-ранк-тесту було встановлено, що кращий результат місцевого лікування виразки відзначався при використанні досліджуваного препарату в порівнянні зі стандартною терапією (p = 0,017). Регресійний аналіз Кокса показав, що використання досліджуваного препарату підвищувало шанс повного загоєння виразкового дефекту в 3,46 рази (95% CI 1,10; 10,83), p = 0,033, на будь-якому часовому відрізку лікування. Дане дослідження переконливо продемонструвало ефективність бета-1,3 / 1,6-глюкана і його здатність скорочувати період загоєння виразки. Відсутність небажаних явищ свідчить про безпеку даного препарату.
Довжина виразки в групах порівняння на 1-й (р = 0,203) і на 13-му тижні (р = 0,379) достовірно не розрізнялася, але достовірно відрізнялася в середині лікувальної фази на 7-му тижні (р = 0,030) з меншим показником в досліджуваній групі (рис. 1). Ширина виразки на момент початку терапії (р = 0,143) і при закінченні (р = 0,588) значимо не розрізнялися, але достовірне зменшення ширини виразки відзначили в лікувальній групі на 7-му тижні (р = 0,030) (рис. 1). Динаміка щотижневого зменшення глибини виразки в групах порівняння не мала достовірних відмінностей.

Ми виявили, що під впливом препарату достовірно зменшувалися довжина, ширина і площа виразки в період з 1-го по 7-ю тижня лікування в порівнянні з результатами в групі контролю. Таким чином, результати пілотного дослідження підтвердили нашу гіпотезу про можливість застосування досліджуваного препарату для місцевого лікування трофічних виразок нижніх кінцівок у хворих на цукровий діабет, що стало підставою для виконання другої фази дослідження.
Результати 2-ї фази дослідження переконливо продемонстрували, що трофічна виразка нижньої кінцівки вірогідно швидше заживала в групі лікування, в якій середній час склало 56 днів (Md = 56,00; 35,00; 84,00), в той час як в групі плацебо - 84 дня (Md = 84,00; 77,00; 84,00, р = 0,019). В межах фази лікування протягом 12 тижнів в групі досліджуваного препарату повністю зажили 14 виразок, а в групі плацебо - тільки 7 виразок при спочатку порівнянних розмірах трофічної виразки в обох групах. При аналізі часу загоєння виразок за допомогою «кривих виживаності» Каплана - Майера і лог-ранк-тесту було встановлено, що кращий результат був у випадках використання досліджуваного препарату, що наноситься безпосередньо на область виразки, ніж при використанні плацебо (p = 0,018) (рис . 2). Регресійний аналіз Кокса дозволив встановити, що місцеве застосування бета-1,3 / 1,6-глюкана достовірно підвищувало шанс повного загоєння виразкового дефекту в 2,78 рази (95% CI 1,12; 6,92), p = 0,028, на будь-якому відрізку часу процесу загоєння.

У випадках використання препарату гель бета-1,3 / 1,6-глюкана не було зафіксовано небажаних явищ, в той час як в контрольній групі відбулися несприятливі події: у 4 пацієнтів розвинувся остеомієліт пальців з подальшою ампутацією, у 2 - флегмона стопи. Також безпеку застосування препарату була підтверджена результатами біохімічних досліджень, виконаних після закінчення лікування.
При включенні пацієнтів в дослідження довжина виразки в обох групах достовірно не розрізнялася (р = 0,126), було зареєстровано більш швидке зменшення розмірів виразки до середини лікування (р = 0,036) і до кінця дослідження (р = 0,029), з достовірними змінами тільки в групі досліджуваного препарату (рис. 3). При включенні пацієнтів в дослідження площа виразки в обох групах також достовірно не розрізнялася (р = 0,119). У процесі лікувальної фази було відзначено достовірне зменшення площі виразки на 7-й (р = 0,046) і на 13-му тижні лікування (р = 0,036) в групі досліджуваного препарату (рис. 3).

При включенні пацієнтів в дослідження обсяг виразки в обох групах достовірно не відрізнявся (р = 0,252). У процесі лікувальної фази достовірна різниця зменшення обсягу виразки з'явилася на 7-й (р = 0,023) і на 13-му тижні лікування (р = 0,044) в групі досліджуваного препарату. При проведенні парного порівняння динаміки зменшення глибини виразки всередині кожної групи були отримані дані про більш швидкому зменшенні цього показника в групі досліджуваного препарату, особливо виразне в період з 1-го по 7-ю тижня лікування (Z = -2,86, р = 0,004 ) і з 7-ї по 13-й тиждень (Z = -2,46, р = 0,014). У групі плацебо достовірного зниження глибини виразки в ці періоди лікування не спостерігалося (Z = -1,23, р = 0,219).
До кінця 12-го тижня лікування в групі досліджуваного препарату не зажили 7 виразкових дефектів, а в групі плацебо - 14. Достовірних відмінностей за розмірами виразки до кінця лікувальної фази не відзначалося, але при застосуванні досліджуваного препарату кінцеві параметри виразки були менше, ніж при терапії плацебо (табл. 6). Також відзначалася статистична тенденція до зниження показників, що відображають наявність запального процесу в організмі в групі досліджуваного препарату, про що свідчили більш низькі середні показники СРБ і ШОЕ, на відміну від групи плацебо.

Після завершення 2-ї фази плацебо-контрольованого дослідження ми продовжили спостереження за хворими протягом наступного року. В аналізований проміжок часу в лікувальній групі з незагоєних 7 виразок в 4 випадках виразки повністю закрилися, одна зараза не зажила і були виконані 2 ампутації пальців стопи. У групі плацебо з 14 незагоєних виразок 5 зажили, 4 - не загоїлися протягом року і було виконано 5 малих ампутацій. Таким чином, в цілому в цій групі з 42 пацієнтів 5 виразок (11,9%) не зажили і протягом наступного року лікування. У цих пацієнтів було виконано 7 малих ампутацій, що склало 16,6%. Через рік після виконання дослідження в групі досліджуваного препарату малі ампутації були виконані в 8,33% випадків, а в групі плацебо - в 19,44% (c2 (1) = 1,65, р = 0,199). Відносний ризик виконання ампутацій виявився в групі досліджуваного препарату в 2,09 рази менше, ніж у контрольній групі плацебо (RR = 2,09, 95% СI 0,64-6,82). У групі досліджуваного препарату знову через рік з'явилися трофічні виразки в 8,82% випадків, а в групі плацебо виникнення нових виразок було в 20,59% випадків (c2 (1) = 1,66, р = 0,198), тобто в 2 , 3 рази більше, ніж в групі пацієнтів, які отримували препарат. Відносний ризик появи нових виразок виявився в 2,07 рази менше в групі досліджуваного препарату, ніж в групі плацебо (RR = 2,07, 95% СI 0,64-6,70).
З метою оцінки впливу препарату бета-1,3 / 1,6-глюкана на час, потрібний для повного загоєння виразки, ми об'єднали бази даних по двох фаз дослідження: пілотної і з аналізом часу загоєння за допомогою кривих виживання Каплана - Майера і лог- ранк-тесту. Ми встановили значне прискорення процесу загоєння в групі застосування досліджуваного препарату протягом 12-тижневої лікувальної фази (р = 0,01). Як випливає з графіка кривих виживаності Каплана - Майера, ймовірність загоєння виразки за 12-тижневий період лікування (до 84-го дня) в групах порівняння була різною. У групі без використання досліджуваного препарату, ця ймовірність була менше 40%, а в групі досліджуваного препарату вона склала майже 80%. Регресійний аналіз Кокса показав, що місцеве застосування бета-1,3 / 1,6-глюкана підвищувало шанс повного загоєння виразкового дефекту в 3,08 рази (95% CI 1,52-6,28) (p = 0,002) на будь-якому відрізку лікування.
Для подальшої оцінки факторів, що впливають на загоєння виразки, все виразки нижніх кінцівок розділили на 3 групи: нейропатичні, нейроішеміческіе і виразки нижньої третини гомілки. До групи хворих з нейропатической виразкою увійшли 33 пацієнта, з них 19 чоловік отримували в якості додаткової місцевої терапії на область виразки гель бета-1,3 / 1,6-глюкана. Згідно з даними регресійного аналізу в цій групі ймовірність загоєння виразки була в 2,27 (1,00; 5,37) рази вище, ніж в групі плацебо. Швидкість загоєння при використанні досліджуваного препарату була також достовірно більше при оцінці кривих виживаності (p = 0,042). У групі нейроішеміческіе виразки, що складалася з 18 хворих, 11 пацієнтів отримували місцево на область виразки досліджуваний препарат. Швидкість загоєння нейроішеміческіе виразки при використанні досліджуваного препарату була також більше, ніж в групі без його використання (р = 0,049), але вплив досліджуваного препарату було менш достовірним, хоча і відзначалася впевнена статистична тенденція до збільшення шансу досягнення кінцевої точки в 6,1 рази ( 0,75; 49,69) в групі досліджуваного препарату. Ми вважаємо, що при збільшенні обсягу вибірки статистична значимість ймовірності загоєння нейроішеміческіе виразки, можливо, могла б посилитися. У групі трофічних виразок з локалізацією в області нижньої третини гомілки було 14 пацієнтів, при цьому велика частина (10 чол.) Входили в групу контролю і не отримували досліджуваний препарат. При аналізі швидкості загоєння визначалася позитивна тенденція досягнення кінцевої точки в групі лікування (р = 0,077), але при використанні кривих виживаності статистична тенденція не досягла достовірності через недостатню вибірки. За допомогою регресійного аналізу для оцінки можливості досліджуваного препарату збільшувати швидкість загоєння виразки також була виявлена тільки статистична тенденція до прискорення цього процесу в 4,1 рази (0,68; 24,63) в порівнянні з терапією без нього.
Крім впливу досліджуваного препарату на швидкість загоєння трофічної виразки при цукровому діабеті ми вивчали деякі інші клінічні предиктори, що прискорюють або сповільнюють цей процес. Для визначення значущих чинників загоєння був обраний регресійний аналіз Кокса, який дозволив нам проаналізувати вплив кожного предиктора окремо на процес загоєння трофічної виразки в залежності від кількості витрачених на лікування днів (в нашому випадку 84 дня). При визначенні значущих предикторів для загоєння виразки ми використовували кожен фактор в регресії по черзі і виявляли достовірність отриманих коефіцієнтів. Серед клініко-антропометричних показників пацієнтів негативно впливали на швидкість загоєння виразки стаж цукрового діабету (HR = 0,93, 95% CI 0,89-0,97) і рівень систолічного системного артеріального тиску (HR = 0,98, 95% CI 0 , 97-0,99). На процес загоєння трофічної виразки негативно впливали швидкість осідання еритроцитів, що визначається до початку лікування (HR = 0,97, 95% CI 0,95-0,99), і вихідний рівень креатиніну (HR = 0,001, 95% CI 0,001-0,768) . У той же час приблизно клінічно значущі при цукровому діабеті чинники, такі як ступінь компенсації цукрового діабету на підставі рівня глікозильованого гемоглобіну (HR = 1,02, 95% CI 0,85-1,23); лейкоцитоз (HR = 0,88, 95% CI 0,77-1,002); С-реактивний білок (HR = 0,99, 95% CI 0,98-1,01), не опинилися предикторами, достовірно впливають на швидкість загоєння виразки. У нашій вибірці вихідний рівень креатиніну негативно впливав на швидкість загоєння виразки, хоча його значення було мінімальним, а при подальшому аналізі цей показник не виявився значущим предиктором загоєння. Кореляційний аналіз і лінійний регресійний аналіз не виявили статистично значимого впливу фактора нефропатії - як її наявності, так і відсутності (HR = 1,18, 95% CI 0,62-2,26) - на швидкість загоєння трофічних виразок. Результати виконаних нами досліджень демонструють, що при збільшенні ЛПІ в цифровому значенні шанс того, що загоєння відбудеться швидше, зростає в 12,37 рази (95% СI 2,50-61,17). В цілому при аналізі всієї вибірки виявилося, що нейропатичні (HR = 2,71, 95% CI 1,37-5,38) трофічні виразки заживають швидше, ніж нейроішеміческіе (HR = 0,61, 95% CI 0,28-1 , 33) і виразки з локалізацією в нижній третині гомілки (HR = 0,41, 95% CI 0,16-1,05). У нашій роботі були отримані дані про те, що наявність склерозу Менкеберга негативно позначається на швидкості загоєння трофічної виразки (HR = 0,30, 95% CI 0,12-0,75), що може дещо суперечити загальноприйнятим даними, оскільки наявність кальцинозу дрібних судин стопи розглядається як характерний прояв нейропатических діабетичних виразок. Трофічні виразки гоїлися повільніше, якщо спочатку мали велику довжину (HR = 0,93, 95% CI 0,89-0,98) і ширину (HR = 0,94, 95% CI 0,89-0,99), в той час як глибина виразки не зробила достовірного впливу на швидкість загоєння виразки в обговорюваній вибірці хворих (HR = 0,93, 95% CI 0,81-1,06).
Подальшої нашою метою була побудова математичної моделі прогнозу загоєння, яке виконали при використанні регресійного аналізу Кокса, що враховує часовий чинник загоєння. Всі перераховані вище негативні і позитивні предиктори були включені в регресію і потім автоматично прибиралися найменш значущі з них. В результаті найбільшу предсказательную значимість для прогнозування швидкості загоєння виразкових дефектів мали такі предиктори: досліджуваний препарат бета-1,3 / 1,6-глюкан, стаж цукрового діабету, довжина виразкового дефекту, підвищення систолічного артеріального тиску. Модель була достовірною у визначенні кінцевого результату - ймовірності повного загоєння виразки за певний проміжок часу (-2 LL = 249, 69, c2 (4) = 30,99, p <0,001). У даній моделі внесок кожного фактора був достовірним. При застосуванні досліджуваного гелю швидкість загоєння збільшувалася в 2,59 рази (95% CI 1,24-5,39). Зі збільшенням стажу цукрового діабету на 1 рік швидкість загоєння зменшувалася в 0,93 рази (95% CI 0,89-0,98). Також чим більше була довжина рани в міліметрах до лікування, тим повільніше вона затягувалася, - якщо бути точними, то в 0,95 рази (95% СI 0,91-0,99). Зі збільшенням систолічного артеріального тиску швидкість загоєння виразки зменшувалася в 0,98 рази (95% CI 0,97-0,99).
У нашій моделі була невелика кількість предикторів, але вона є самий корінь. Для даної потужності вибірки обстежених хворих така кількість предикторів оптимально. Застосування цієї моделі в повсякденній практиці не повинно скласти труднощів, є економічно дешевим, але достовірним способом прогнозу загоєння трофічної виразки нижніх кінцівок у хворого на цукровий діабет.
Висновки
1. Клінічний фенотип пацієнта на цукровий діабет і трофічною виразкою нижніх кінцівок характеризується тривалим стажем захворювання, незадовільним контролем метаболізму, наявністю судинних ускладнень, особливо хронічного захворювання нирок і ішемічної хвороби серця, а також склерозу Менкеберга і проявів загального запального синдрому (збільшення ШОЕ, лейкоцитоз, високий рівень СРБ).
2. В Архангельській області на протязі останніх років спостерігалася велика поширеність високих ампутацій нижніх кінцівок у хворих СДС в порівнянні з середніми даними по РФ: при СД 1-го типу - в 3,6 рази частіше, а при ЦД 2-го типу - в 7 раз. Після створення кабінету «Діабетична стопа» і впровадження сучасного стандарту лікування трофічних діабетичних виразок нижніх кінцівок, що базується на основі міждисциплінарного підходу і наступності надання допомоги, протягом наступних трьох років (2006-2008 рр.) В м Архангельську в 2 рази знизилася частота великих ампутацій - з 63,2 до 38,5%.
3. Швидкість репаративного процесу трофічної діабетичної виразки нижньої кінцівки, а також шанси її загоєння достовірно збільшувалися при використанні в якості місцевого лікування гелю розчинної бета-1,3 / 1,6-глюкана з медіаною часу до кінцевої точки 35 днів, в той час як при стандартному лікуванні і використанні плацебо цей процес займав 84 дня.
4. У групах застосування досліджуваного препарату були відсутні небажані явища і ознаки токсичності, що дозволило зробити висновок про безпеку даного препарату при достовірному прискоренні процесу загоєння в середньому більш ніж в 3 рази.
Клінічно значимими предикторами швидкості загоєння виявилися ЛПІ і систолічний артеріальний тиск, стаж СД, склероз Менкеберга, а також ширина і довжина виразки, показник ШОЕ, збільшення яких знижувало швидкість загоєння, в той час як вона збільшувалася при нейропатической виразці і застосуванні досліджуваного препарату, внесок якого був істотним і достовірним.


