- Йога начинающим видео
- Хулахуп танец видео
- Смотреть моя тренировка видео
- Видео тренировки александра емельяненко
- Как правильно крутить обруч на бедрах видео
- Тренировки в кудо видео
- Тренировки рой джонса видео
- Йога онлайн смотреть видео
- Тренировки костя дзю видео
- Видео тренировки роя джонса
- Видео спинальной
- Айенгар йога видео
- Йога для женщин на видео
- Правильно крутить обруч видео
- Плиометрические отжимания видео
- Новости

Управление Здравоохранения Евпаторийского городского совета (С)2011
67 гостей
Оцтова кислота
- У промисловості [ правити | правити код ]
- Каталітичне карбонилирования метанолу [ правити | правити код ]
- Біохімічний спосіб виробництва [ правити | правити код ]
- Гідратація ацетилену в присутності ртуті і двовалентних солей ртуті [ правити | правити код ]
- Оцтова кислота в біохімії організмів [ правити | правити код ]
Оцтова кислота 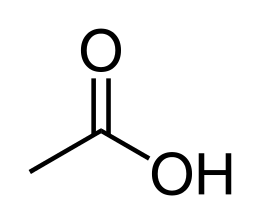
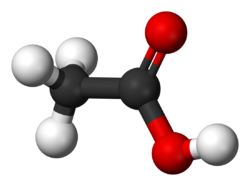
 систематичне
систематичне
найменування Метанова кислота Традиційні назви Оцтова кислота Хім. формула C2H4O2 Рац. формула CH3COOH стан рідина молярна маса 60,05 г / моль щільність 1,0492 г / см³ Поверхневий натяг 27,1 ± 0,01 мН / м [1] , 24,61 ± 0,01 мН / м [1] і 22,13 ± 0,01 мН / м [1] динамічна в'язкість 1,056 мПа · с [2] , 0,786 мПа · с [2] , 0,599 мПа · с [2] і 0,464 мПа · с [2] енергія іонізації 10,66 ± 0,01 еВ [3] Т. плав. 16,75 ° C Т. кип. 118,1 ° C Т. доп. 103 ± 1 ° F [3] і 39 ± 6 ° C [4] Т. свспл. 427 ± 1 ° C [5] Пр. взрв. 4 ± 0,1 об.% [3] Кр. крапка 321,6 ° C, 5,79 МПа Мовляв. теплоємність. 123,4 Дж / (моль · К) ентальпія освіти -487 кДж / моль Тиск пара 11 ± 1 мм рт.ст. [3] , 10 ± 1 кПа [6] і 100 ± 1 кПа [6] pKa 4,76 (Ka = 1,75 * 10-5) Показник заломлення 1,372 дипольний момент 1,74 Д Реєстр. номер CAS 64-19-7 PubChem 176 Реєстр. номер EINECS 200-580-7 SMILES InChI Кодекс Аліментаріус E260 RTECS AF1225000 ChEBI 15366 номер ООН 2789 ChemSpider 171 токсичність  NFPA 704 Наводяться дані для стандартних умов (25 ° C, 100 кПа) , Якщо не вказано іншого.
NFPA 704 Наводяться дані для стандартних умов (25 ° C, 100 кПа) , Якщо не вказано іншого.
Оцтова кислота (метанова кислота) CH3COOH - органічна сполука , Cлабо, гранична одноосновная карбонова кислота . Солі та складні ефіри оцтової кислоти називаються ацетатами .
оцет є продуктом бродіння вина і відомий людині з давніх часів.
Перша згадка про практичне застосування оцтової кислоти відноситься до III століття до н. е. грецький вчений Теофраст вперше описав дію оцту на метали , Що приводить до утворення деяких використовуваних в мистецтві пігментів . Оцет застосовувався для отримання свинцевих білил , а також ярь-мідянки (Зеленої суміші солей міді, що містить крім усього ацетат міді).
У Стародавньому Римі готували спеціально кисле вино в свинцевих горщиках. В результаті виходив дуже солодкий напій, який називали «сапа». Сапа містила велику кількість ацетату свинцю - дуже солодкого речовини, яке також називають свинцевим цукром або цукром Сатурна . Висока популярність сапи була причиною хронічного отруєння свинцем , Поширеного серед римської аристократії [7] .
У VIII столітті арабський алхімік Джабір ібн Хайян вперше виклав способи отримання оцту.
В часи епохи Відродження оцтову кислоту отримували шляхом сублімації ацетатів деяких металів (найчастіше використовувався ацетат міді (II)) (при сухий перегонці ацетатов металів виходить ацетон, цілком промисловий спосіб до середини XX століття).
Властивості оцтової кислоти змінюються в залежності від вмісту в ній води . У зв'язку з цим багато століть хіміки помилково вважали, що кислота з вина і кислота з ацетатов є двома різними речовинами. Ідентичність речовин, отриманих різними способами, була показана німецьким алхіміком XVI століття Андреасом Лібавіусом ( ньому. Andreas Libavius) і французьким хіміком П'єром Огюстом Аді ( фр. Pierre Auguste Adet) [7] .
В 1847 році німецький хімік Адольф Кольбе вперше синтезував оцтову кислоту з неорганічних матеріалів. Послідовність перетворень включала в себе хлорування сірковуглецю до тетрахлорметана з подальшим пиролизом до тетрахлоретилену. Подальше хлорування в воді призвело до трихлоруксусной кислоті, яка після електролітичного відновлення перетворилася в оцтову кислоту [8] .
В кінці XIX - початку XX століття більшу частину оцтової кислоти отримували перегонкою деревини . Основним виробником оцтової кислоти була Німеччина . В 1910 році нею було вироблено понад 10 тисяч тонн кислоти, причому близько 30% цієї кількості було витрачено на виробництво барвника індиго [7] [9] .
Оцтова кислота являє собою безбарвну рідина з характерним різким запахом і кислим смаком . гігроскопічна . Необмежено розчинна в воді . Змішується з багатьма розчинниками ; в оцтової кислоти добре розчинні неорганічні сполуки і гази, такі як HF , HCl , HBr , HI та інші. Існує у вигляді циклічних і лінійних димарів [10] .
Абсолютна оцтова кислота називається крижаний, так як при замерзанні утворює льдовідную масу. Спосіб отримання крижаної оцтової кислоти в 1789 році відкрив російський хімік німецького походження Товій Єгорович Ловиц .
- тиск парів (в мм. рт. ст. ):
- 10 (+17,1 ° C)
- 40 (+42,4 ° C)
- 100 (+62,2 ° C)
- 400 (+98,1 ° C)
- 560 (+109 ° C)
- 1520 (+143,5 ° C)
- 3800 (+180,3 ° C)
- Відносна діелектрична проникність : 6,15 (+20 ° C)
- динамічна в'язкість рідин і газів (в мПа · с): 1,155 (+25,2 ° C); 0,79 (+50 ° C)
- Поверхневий натяг : 27,8 мН / м (+20 ° C)
- питома теплоємність при постійному тиску: 2,01 Дж / г · K (+17 ° C)
- стандартна енергія Гіббса освіти ΔfG0 (298 К, кДж / моль): -392,5 (ж)
- стандартна ентропія освіти ΔfS0 (298 К, Дж / моль · K): 159,8 (ж)
- Ентальпія плавлення ΔHпл: 11,53 кДж / моль
- Температура спалаху в повітрі: +38 ° C
- Температура самозаймання на повітрі: 454 ° C
- Теплота спалювання : 876,1 кДж / моль
Оцтова кислота утворює подвійні азеотропні суміші з наступними речовинами.
Речовина температуру кипіння, ° C масова частка оцтової кислоти чотирихлористий вуглець 76,5 3% циклогексан 81,8 6,3% бензол 88,05 2% толуол 104,9 34% гептан 91,9 33% трихлоретилен 86,5 4% етилбензол 114,65 66% о-ксилол 116 76% п-ксилол 115,25 72% бромоформ 118 83%
- Оцтова кислота утворює потрійні азеотропні суміші
У промисловості [ правити | правити код ]
Ранніми промисловими методами отримання оцтової кислоти були окислення ацетальдегіду і бутану [11] .
Ацетальдегід окислюється в присутності ацетату марганцю (II) при підвищеній температурі і тиску. Вихід оцтової кислоти становив близько 95% при температурі + 50- + 60 ° С.
2 C H 3 C H O + O 2 ⟶ 2 C H 3 C O O H {\ displaystyle {\ mathsf {2CH_ {3} CHO + O_ {2} \ longrightarrow 2CH_ {3} COOH}}}
окислення н- бутану проводилося при 150 атм . Каталізатором цього процесу був ацетат кобальту .
2 C 4 H 10 + 5 O 2 ⟶ 4 CH 3 COOH + 2 H 2 O {\ displaystyle {\ mathsf {2C_ {4} H_ {10} + 5O_ {2} \ longrightarrow 4CH_ {3} COOH + 2H_ {2 } O}}}
Обидва методи базувалися на окисленні продуктів крекінгу нафти . В результаті підвищення цін на нафту обидва методи стали економічно невигідними, і були витіснені більш досконалими каталітичними процесами карбонилирования метанолу [11] .
Каталітичне карбонилирования метанолу [ правити | правити код ]
Важливим способом промислового синтезу оцтової кислоти є каталітичне карбонилирования метанолу моноксидом вуглецю [12] , Яке відбувається за формальною рівняння:
C H 3 O H + C O ⟶ C H 3 C O O H {\ displaystyle {\ mathsf {CH_ {3} OH + CO \ longrightarrow CH_ {3} COOH}}}
Реакція карбонилирования метанолу була відкрита вченими фірми BASF в 1913 році. У 1960 році ця компанія запустила перший завод, що виробляє оцтову кислоту цим методом. [13] Каталізатором перетворення служив йодид кобальту. Метод полягав в барботаже монооксиду вуглецю при температурі 180 ° С і тиску 200-700 атм через суміш реагентів. Вихід оцтової кислоти становить 90% по метанолу і 70% по СО. Одна з установок була побудована в Гейсмара (шт. Луїзіана ) І довго залишалася єдиним процесом BASF в США [14] .
Удосконалена реакція синтезу оцтової кислоти карбонілюванням метанолу була впроваджена дослідниками фірми Monsanto в 1970 році . [15] [16] Це гомогенний процес, в якому використовуються солі родію в якості каталізаторів, а також йодид-іони в якості промоторів. Важливою особливістю методу є велика швидкість, а також висока селективність (99% по метанолу і 90% по CO). [11]
Цим способом отримують трохи більше 50% всієї промислової оцтової кислоти. [17]
В процесі фірми BP в якості каталізаторів використовуються з'єднання іридію .
Біохімічний спосіб виробництва [ правити | правити код ]
При біохімічному виробництві оцтової кислоти використовується здатність деяких мікроорганізмів окисляти етанол . Цей процес називають оцтовокислим бродінням. В якості сировини використовуються етанолвмісних рідини ( вино , заграв соки ), Або ж просто водний розчин етилового спирту [18] .
реакція окислення етанолу до оцтової кислоти протікає за участю ферменту алкогольдегідрогенази . Це складний багатоступінчастий процес, який описується формальним рівнянням [19] :
CH 3 CH 2 OH + O 2 → CH 3 COOH + H 2 O {\ displaystyle {\ mathsf {CH_ {3} CH_ {2} OH + O_ {2} \ rightarrow CH_ {3} COOH + H_ {2} O }}}
Гідратація ацетилену в присутності ртуті і двовалентних солей ртуті [ правити | правити код ]
C 2 H 2 + H 2 O → H g 2 + CH 3 CHO {\ displaystyle {\ mathsf {C_ {2} H_ {2} + H_ {2} O {\ xrightarrow [{}] {Hg ^ {2 + }}} CH_ {3} CHO}}} - реакція Кучерова CH 3 CHO → C r O 3, H 2 SO 4 CH 3 COOH {\ displaystyle {\ mathsf {CH_ {3} CHO {\ xrightarrow [{}] {CrO_ {3}, H_ {2} SO_ {4}} } CH_ {3} COOH}}}
Оцтова кислота має всі властивості карбонових кислот , І іноді розглядається як їх найбільш типовий представник (на відміну від мурашиної кислоти , Яка має деякі властивості альдегідів ). Зв'язок між воднем і киснем карбоксильної групи (-COOH) карбонової кислоти є сильно полярної, внаслідок чого ці сполуки здатні легко диссоциировать і проявляють кислотні властивості.

В результаті дисоціації оцтової кислоти утворюється ацетат-іон CH3COO- і протон H +. Оцтова кислота є слабкою одноосновної кислотою зі значенням pKa у водному розчині рівним 4,75. Розчин з концентрацією 1,0 M (Приблизна концентрація харчового оцту) має pH 2,4, що відповідає ступеня дисоціації 0,4%.
На слабкою дисоціації оцтової кислоти у водному розчині заснована якісна реакція на наявність солей оцтової кислоти: до розчину додається сильна кислота (наприклад, сірчана ), Якщо з'являється запах оцтової кислоти, значить, сіль оцтової кислоти в розчині присутній (кислотні залишки оцтової кислоти, що утворилися з солі, зв'язалися з катіонами водню від сильної кислоти і вийшло велика кількість молекул оцтової кислоти) [20] .
Дослідження показують, що в кристалічному стані молекули утворюють димери, пов'язані водневими зв'язками [21] .
Оцтова кислота здатна взаємодіяти з активними металами. При цьому виділяється водень і утворюються солі - ацетати :
M g + 2 CH 3 COOH → (CH 3 COO) 2 M g + H 2 ↑ {\ displaystyle {\ mathsf {Mg + 2CH_ {3} COOH \ rightarrow (CH_ {3} COO) _ {2} Mg + H_ {2} \ uparrow}}}
Оцтова кислота може хлоруватися дією газоподібного хлору. При цьому утворюється хлоруксусная кислота:
C H 3 C O O H + C l 2 → C H 2 C l C O O H + H C l {\ displaystyle {\ mathsf {CH_ {3} COOH + Cl_ {2} \ rightarrow CH_ {2} ClCOOH + HCl}}}
Цим шляхом можуть бути отримані також діхлоруксусной (CHCl2COOH) і трихлоруксусная (CCl3COOH) кислоти.
Оцтова кислота може бути відновлена до етанолу дією алюмогідріда літію . Вона також може бути перетворена в хлорангидрид дією тіонілхлориду . Натрієва сіль оцтової кислоти декарбоксилируется при нагріванні з лугом, що призводить до утворення метану і карбонату натрію .
Оцтова кислота в біохімії організмів [ правити | правити код ]
Оцтова кислота утворюється в живих організмах в процесі вуглеводного обміну , В тому числі в організмі людини в процесі біохімічних реакції, зокрема в циклі Кребса , утилізації алкоголю .
Оцтову кислоту, концентрація якої близька до 100%, називають крижаною. 70-80% -й водний розчин оцтової кислоти називають оцтовою есенцією, а 3-15% -й - оцтом [22] . Водні розчини оцтової кислоти використовуються в харчовій промисловості ( харчова добавка E260) і побутової кулінарії, а також в консервуванні та для позбавлення від накипу. Однак кількість оцтової кислоти, яку використовують як оцту, дуже мало, в порівнянні з кількістю оцтової кислоти, використовуваної в великотоннажному хімічному виробництві.
Оцтову кислоту застосовують для одержання лікарських і запашних речовин, таких як розчинник (Наприклад, у виробництві ацетилцелюлози , ацетону ). Вона використовується в книгодрукуванні і фарбуванні.
Оцтова кислота використовується як реакційна середу для проведення окислення різних органічних речовин. У лабораторних умовах це, наприклад, окислення органічних сульфідів пероксидом водню , В промисловості - окислення пара-ксилолу киснем повітря в терефталевую кислоту .
Оскільки пари оцтової кислоти володіють різким запахом дратівливим, можливо її застосування в медичних цілях у якості заміни нашатирного спирту для виведення хворого з непритомного стану.
Безвода оцтова кислота - їдка речовина. Пари оцтової кислоти подразнюють слизові оболонки верхніх дихальних шляхів. Поріг сприйняття запаху оцтової кислоти в повітрі знаходиться в районі 0,4 мг / л. Гранично допустима концентрація в атмосферному повітрі становить 0,06 мг / м³, в повітрі робочих приміщень - 5 мг / м³ [10] .
Дія оцтової кислоти на біологічні тканини залежить від ступеня її розведення водою. Небезпечними вважаються розчини, в яких концентрація кислоти перевищує 30% [10] . Концентрована оцтова кислота здатна викликати хімічні опіки, які ініціюють розвиток коагуляційних некрозів прилеглих тканин різної протяжності і глибини [23] .
Токсикологічні властивості оцтової кислоти не залежать від способу, яким вона була отримана [24] . Смертельна разова доза становить приблизно 20 мл (при ентеральному прийомі в перерахунку на 100% кислоту).
Наслідками прийому всередину концентрованої оцтової кислоти є важкий опік слизової оболонки порожнини рота, глотки , стравоходу і шлунка ; наслідки всмоктування оцтової есенції - ацидоз , гемоліз , гемоглобинурия , Порушення згортання крові, що супроводжується важкими шлунково-кишковими кровотечами. Характерно значне згущення крові через втрату плазми через обпалену слизову оболонку, що може викликати шок . До небезпечних ускладнень отруєння оцтовою есенцією відносяться гостра ниркова недостатність і токсична дистрофія печінки .
У якості першої допомоги при прийомі оцтової кислоти всередину слід випити велику кількість рідини. Виклик блювоти є вкрай небезпечним, так як вторинне проходження кислоти по стравоходу посилить опік, також кисле вміст може потрапити в дихальні шляхи. Допускається з метою нейтралізації кислоти і захисту слизової прийом паленої магнезії , Сирого яєчного білка, киселю. Не можна вживати з цією метою соду , Так як утворюється вуглекислий газ і вспенивание буде також сприяти ввезенню кислоти назад в стравохід, гортань, а також може призвести до прориву стінок шлунка. Показано промивання шлунка через зонд. Необхідна негайна госпіталізація.
При інгаляційному отруєнні парами потрібно обполоснути слизові водою або 2% розчином харчової соди , Прийом всередину молока, слабкого лужного розчину (2% сода, лужні мінеральні води) з подальшою госпіталізацією.
- ↑ 1 2 3 CRC Handbook of Chemistry and Physics / WM Haynes - 95 - Boca Raton : CRC Press , 2014. - P. 6-182. - ISBN 978-1-4822-0868-9
- ↑ 1 2 3 4 CRC Handbook of Chemistry and Physics / WM Haynes - 95 - Boca Raton : CRC Press , 2014. - P. 6-232. - ISBN 978-1-4822-0868-9
- ↑ 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0002.html
- ↑ CRC Handbook of Chemistry and Physics / WM Haynes - 95 - Boca Raton : CRC Press , 2014. - P. 16-19. - ISBN 978-1-4822-0868-9
- ↑ http://www.cdc.gov/niosh/ipcsneng/neng0363.html
- ↑ 1 2 CRC Handbook of Chemistry and Physics / WM Haynes - 95 - Boca Raton : CRC Press , 2014. - P. 6-95. - ISBN 978-1-4822-0868-9
- ↑ 1 2 3 Martin, Geoffrey. Industrial and Manufacturing Chemistry. - Part 1, Organic. - London: Crosby Lockwood, 1917. - P. pp. 330-31.
- ↑ Goldwhite, Harold. Short summary of the career of the German organic chemist, Hermann Kolbe (Англ.) // New Haven Section Bull. Am. Chem. Soc. : Journal. - 2003. - September (vol. 20, no. 3).
- ↑ Schweppe, Helmut. Identification of dyes on old textiles (Неопр.) // J. Am. Inst. Conservation. - 1979. - Т. 19, № 1/3. - С. 14-23. - DOI : 10.2307 / 3179569 .
- ↑ 1 2 3 Оцтова кислота
- ↑ 1 2 3 Реутов О. А. Органічна хімія. - М.: Изд-во МГУ, 1999. - Т. 4.
- ↑ Advances in Organometallic Chemistry
- ↑ Acetic Acid Production and Manufacturing Process
- ↑ Б. Лич. Каталіз в промисловості. Том 1. - Москва: Мир, 1986. - 324 с.
- ↑ US Patent 3 769 329
- ↑ патент США
- ↑ Екологічний фактор, або Довкілля як стимул еволюції промислової хімії
- ↑ Кандидат біологічних наук Н. Кустова. Оцет. Що це таке і як його роблять (Рос.). Інтернет-ресурс «Всяка всячина». Дата обігу 2 вересня 2010 року. Читальний зал 26 серпня 2011 року.
- ↑ Біотехнологія органічних кислот і білкових препаратів: Навчальний посібник
- ↑ Ходаков Ю. В., Епштейн Д. А., глоріоза П. А. § 8. Реакції іонного обміну // Неорганическая хімія. Підручник для 9 класу. - 7-е вид. - М.: Просвітництво , 1976. - С. 15-18. - 2 350 000 прим.
- ↑ Jones, RE; Templeton, DH The crystal structure of acetic acid (англ.) // Acta Crystallogr. (Англ.): Journal. - International Union of Crystallography , 1958. - Vol. 11, no. 7. - P. 484-87. - DOI : 10.1107 / S0365110X58001341 .
- ↑ Оцет - стаття з Великої радянської енциклопедії .
- ↑ Оцтова кислота: Медичний портал Eurolab
- ↑ www.textra-vita.com/technology Глава 17. Оцтова кислота 7. Токсиколого-гігієнічна оцінка


